探讨与争鸣
细胞外基质(ECM)
古老生命的“脚手架”,现代科学的“新大陆”
2025年09月05日 10:12
当你不小心划破手指时,是否好奇过伤口如何神奇愈合?这背后是一场由细胞外基质(ECM)导演的“生命交响曲”。ECM曾被视为简单的“细胞胶水”,如今却被科学界重新定义为“智能生物计算机”—它不仅能像古老建筑的脚手架一样支撑组织,更能通过分子信号“指挥”细胞行为。对比传统认知,现代研究发现:ECM的“失效”是皮肤老化(胶原流失)、慢性伤口(如糖尿病足)甚至癌症转移的关键因素。而对消费者而言,理解ECM或许能回答一个终极问题:为什么某些护肤品能“治本”,而另一些仅“治标”?
ECM长期以来被视为一种静态的“支架”,其主要功能是为细胞提供机械支撑和结构完整性。传统观点认为,ECM由胶原蛋白(如I型、III型)、纤连蛋白、透明质酸(HA)等成分被动地填充在细胞间隙中,仅仅作为组织结构的“填充物”;对其生物学功能也仅局限于其静态的物理特性,例如胶原蛋白赋予组织强度,透明质酸提供保湿能力。
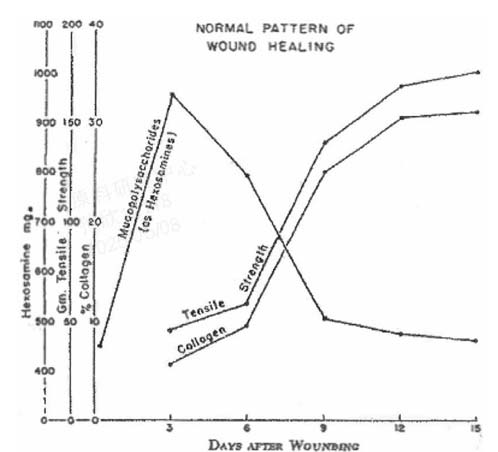
然而,随着研究的深入,尤其是近年来《Nature》等顶级期刊的突破性发现,ECM的角色被重新定义——它是一种高度动态且可编程的“智能材料”[1],能够主动参与并调控组织的修复与再生过程。研究表明[2],ECM的组成和结构会随着组织状态(如损伤、炎症、修复)动态变化(图 1),并通过与细胞的相互作用传递信号,调控细胞行为。例如,胶原蛋白III型(COLIII)在皮肤修复过程中会呈现高表达,为细胞迁移提供临时支架,同时通过结合生长因子调节炎症反应[3];而纤连蛋白作为皮肤损伤后最先沉积的ECM蛋白,它不仅提供粘附位点,还能激活整合素信号通路,促进细胞迁移和增殖[3];而HA的功能高度依赖分子量,低分子量HA通过CD44受体激活促增殖信号,高分子量HA则抑制炎症并维持组织稳态[2]。
华熙生物的研究为ECM的动态性提供了生动例证。重组人源III型胶原(rhCOLIII)与其他ECM成分的组合展现出类似“分子开关”的功能,能够精准调控皮肤修复的不同阶段:
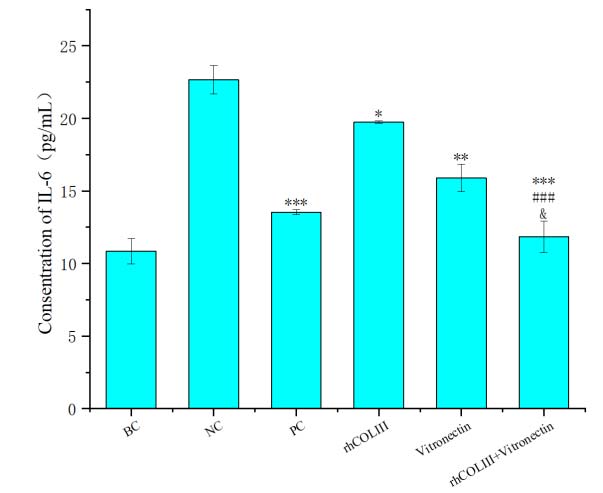
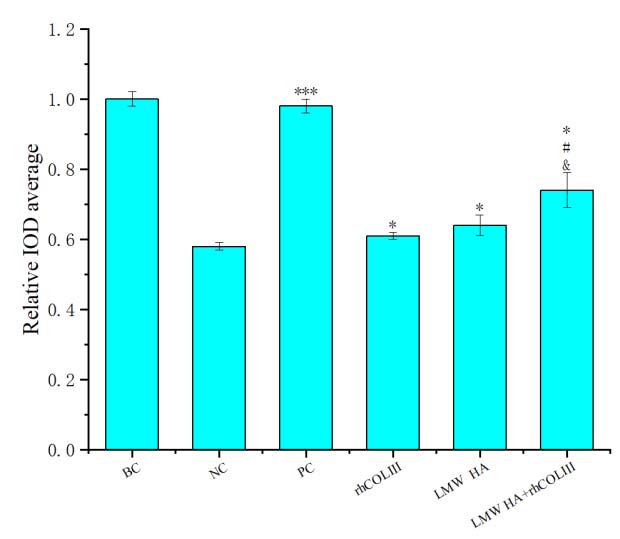
1. 炎症期:rhCOLIII与玻连蛋白(vitronectin)协同显著降低促炎因子IL-6的表达(图 2),避免过度炎症对组织的二次损伤。
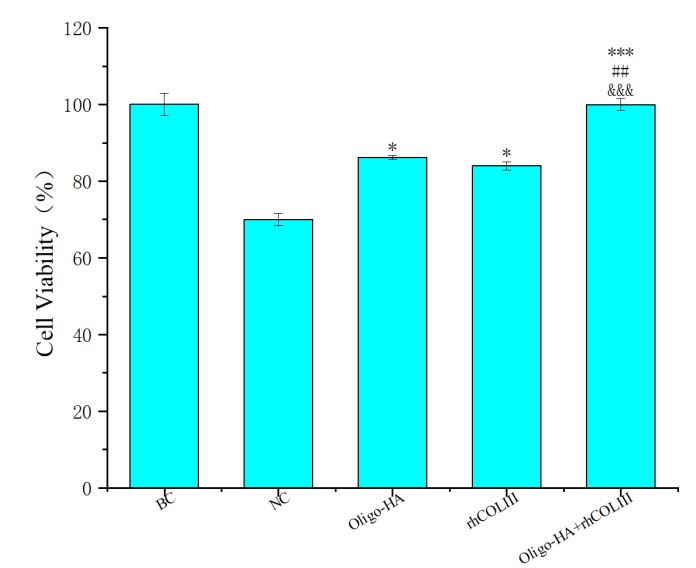
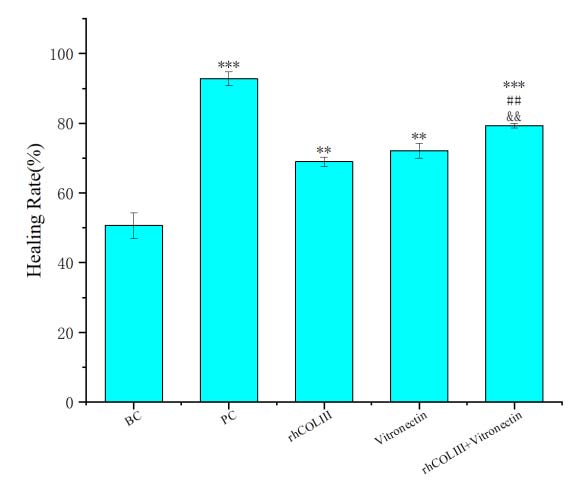
2. 增殖期:rhCOLIII与寡聚HA(oligo-HA)组合协同促进成纤维细胞增殖(图 3)。rhCOLIII与玻连蛋白协同组合协同促进成纤维细胞的迁移(图 5)。
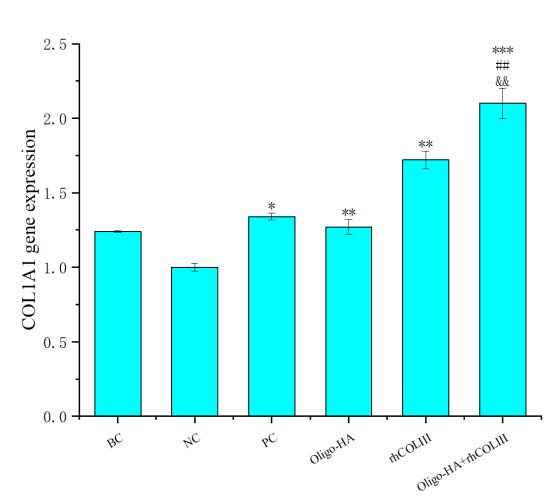
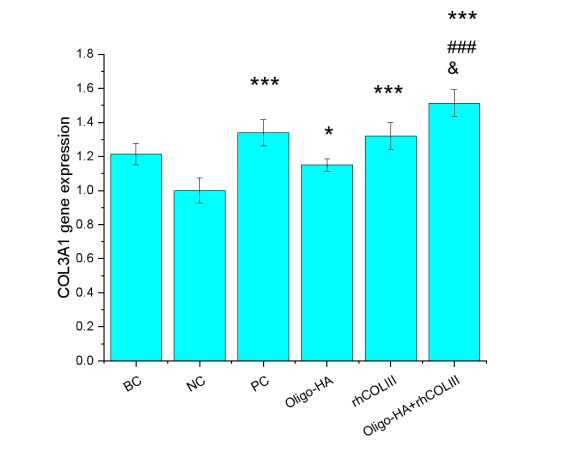
3. 重塑期:rhCOLIII与寡聚HA(oligo-HA)组合通过上调COL1A1和COL3A1基因表达(图 4),促进胶原合成,加速真皮组织重建。rhCOLIII与低分子量HA(LMW-HA)协同增强丝聚蛋白(FLG)表达(图 6),推动角质形成细胞分化,恢复表皮屏障功能。
这种“时序调控”能力使ECM成为修复过程的“时间管理者”,能够根据修复阶段的需求动态调整其组成和功能。
ECM的这种动态特性为生物医学工程提供了新思路,科学家可以通过设计仿生ECM材料,来模拟其“编程”能力[1]。比如,利用HA的分子量依赖性,可以开发阶段性释放药物(如先抑制过度炎症,后促增殖)的智能敷料;通过调控ECM的动态平衡(如增加COLIII/COLⅠ比例),可以延缓皮肤纤维化与衰老。
ECM从“静态支架”到“动态网络”的认知转变,揭示了其在组织修复中的核心地位。ECM作为一种可编程的生物学界面,其与细胞的动态交互能力为再生医学和疾病治疗开辟了新途径。未来,通过解码ECM的“分子语言”,人类或许能够实现组织再生的精准操控,让古老的ECM焕发新的生命力。
透明质酸在细胞外基质中扮演着精密的分子信号传递者角色,其功能多样性主要取决于分子量的精微差异。这种分子量依赖的特性使HA能够像生物密码一样,在皮肤修复的不同阶段传递特定指令。比如,高分子量HA(HMW-HA)在皮肤炎症期,为炎症细胞浸润提供支架,同时抑制炎症因子(如TNF-α)表达,维持组织稳态(如抑制过度炎症反应)。LMW-HA通过HMW-HA经透明质酸酶降解生成,在皮肤修复的增殖期,刺激成纤维细胞增殖和III型胶原合成,推动肉芽组织形成,促进组织重建。由此可见,HMW-HA是“保护伞”,抑制炎症并维持结构;而LMW/oligo-HA是“行动指令”,驱动细胞迁移、增殖和组织重塑[2]。
华熙生物的创新之处在于破解了这套"HA密码系统",并开发出相应的“分阶应用”技术。通过精确控制HA的分子量分布和配伍成分,实现了从基础保湿到促进再生的功能跃迁。比如,在皮肤修复的增殖期用促增殖配方(rhCOLIII+oligo-HA),动员皮肤细胞快速补充到受损部位,而重塑期用促胶原再生+屏障修复方案(rhCOLIII+LMW-HA+ oligo-HA),同步地促进真皮层和表皮层组织的重建,并通过其他ECM成分的干预,使得皮肤组织修复到完好如初的状态。这种“动态编程”逻辑,将HA的分子量差异转化为精准的修复时序控制,形成“识别-响应-修复”的闭环。
未来华熙生物的研究团队将进一步探索HA信号系统的可编程性。环境响应型HA能在特定pH或酶条件下释放治疗性片段;靶向修饰HA通过嫁接特定寡肽增强组织特异性;动态交联HA可随修复进程自主调整基质力学特性。这些创新方向将使HA从被动的ECM组分转变为主动的修复调控者,真正实现对组织再生过程的精准干预。
当科学家学会“重编程”ECM,我们或许将进入“再生医学2.0”时代。细胞外基质(ECM)不再只是被动的结构支架,而是动态调控细胞行为的“生物指令系统”——它决定组织如何修复、衰老,甚至如何对抗疾病。华熙生物的研究揭示了这一潜力,并通过重组III型胶原与特定分子量透明质酸的组合,可精准调控炎症、增殖与重塑阶段,从而优化皮肤修复质量。这种“ECM编程”逻辑,未来可能突破皮肤范畴,延伸至更复杂的医学挑战。
华熙生物的价值,在于将ECM科学从实验室推向生活。当“熬夜面膜”含有修复ECM的活性成分,当术后凝胶能按需释放不同分子量HA,消费者便直接参与了这场“ECM革命”。未来,随着生物打印、基因编辑等技术的成熟,ECM或许会成为医学的“通用操作系统”——就像手机APP依赖iOS/安卓,我们的健康将依赖于对ECM的精准调控。毕竟,最好的科学不仅是发表在顶刊上的突破,更是能“涂抹”在脸上、注射到体内、改写生命轨迹的现实改变。
引用
[1] Xue, Bin, et al. "Hydrogels with programmed spatiotemporal mechanical cues for stem cell-assisted bone regeneration." Nature Communications 16.1 (2025): 3633.
[2] Aya, Kessiena L., and Robert Stern. "Hyaluronan in wound healing: rediscovering a major player." Wound repair and regeneration 22.5 (2014): 579-593.
[3] Potekaev, Nikolai N., et al. "The role of extracellular matrix in skin wound healing." Journal of Clinical Medicine 10.24 (2021): 5947.
本文作者:孙欣,仅代表个人观点。Bioπ中国美肤科学传播平台发布本文只是为了更多的信息参考,不代表任何有倾向性的投资意见或市场暗示。
THE END
指导单位:中国香料香精化妆品工业协会
受托运营:中国香妆融媒体
京ICP备2025131973号

:古老生命的“脚手架”,现代科学的“新大陆-1.jpg)
:古老生命的“脚手架”,现代科学的“新大陆-2.jpg)
:古老生命的“脚手架”,现代科学的“新大陆-3.jpg)







