封面报道
皮肤的塌陷:
细胞外基质变化与皱纹松弛的秘密
2026年01月26日 15:16
当第一道细纹悄然爬上眼角,当肌肤不再紧致如初,我们直观地感受到时光在身体上刻下的印记。这些可见的衰老迹象,并不仅仅是皮肤表层的干燥或暂时的状态不佳,而是一场发生在皮肤深层、关乎其支撑结构的“静悄悄的革命”。这场革命的核心舞台,便是由胶原蛋白、弹性蛋白和糖胺聚糖等构成的“细胞外基质”。
想象一下,年轻的皮肤如同一个由优质弹簧(胶原蛋白和弹性蛋白)和富含水分的气垫(糖胺聚糖,特别是透明质酸)共同支撑的席梦思床垫,饱满而富有弹性。然而,随着年龄增长,内部的弹簧开始生锈、断裂,气垫也逐渐漏气、干瘪。最终,原本平整饱满的床垫表面开始出现凹陷、松弛,这就是皱纹和皮肤松弛诞生的微观比喻。
皮肤衰老是一个复杂的生物学过程,受到内在遗传因素和外在环境因素的双重影响。在这一过程中,细胞外基质的降解与破坏被公认为导致皮肤形态和功能衰退的关键环节。细胞外基质不仅为皮肤细胞提供物理支撑,还积极参与细胞信号传导、组织修复和稳态维持。因此,理解ECM的变化,是揭开皮肤衰老秘密的核心。
本文将以细胞外基质为焦点,深入探讨其在维持皮肤年轻态中的作用,详细解析导致ECM塌陷的内外因素,并系统地介绍当前科学界认可的、能够有效保护和修复ECM的策略。从日常护肤成分的选择到新兴的再生医学技术,我们将为您呈现一份基于最新科学证据的“皮肤支撑结构”维护指南。


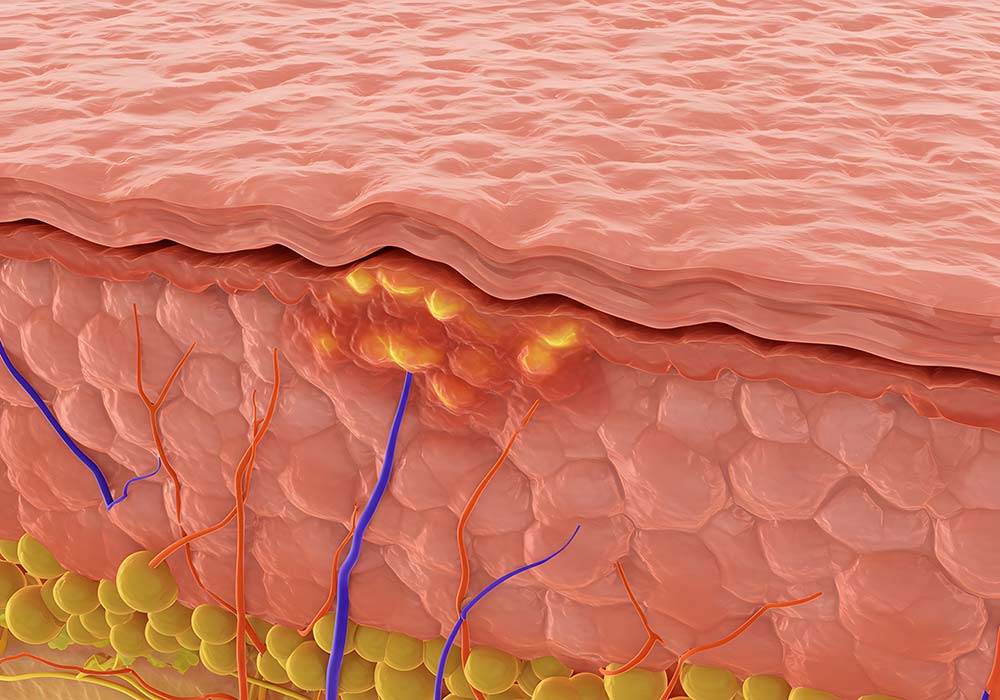
细胞外基质(Extracellular Matrix, ECM)并非惰性的填充物,而是一个由多种大分子构成的动态、复杂的网络结构。它主要由胶原蛋白、弹性蛋白、糖胺聚糖/蛋白聚糖以及纤维连接蛋白等成分组成,共同为皮肤提供结构完整性、弹性和水合作用。
胶原蛋白又被称为皮肤的“钢架结构”,是ECM中最主要的成分,约占皮肤干重的75%-80%。它主要由成纤维细胞合成,形成粗壮的纤维束,为皮肤提供强大的抗张强度和机械支撑。在皮肤中,I型和III型胶原蛋白最为丰富,其中III型胶原在婴幼儿时期占比更高,与皮肤的柔韧性和细腻度相关。胶原蛋白的密度、排列和结构稳定性直接决定了皮肤的紧致度和厚度。随着年龄增长,不仅胶原蛋白的总量减少,其结构也变得杂乱无章,如同朽坏的木材,支撑力大不如前。
弹性蛋白则是皮肤弹性的关键。它构成一个复杂的网络,赋予皮肤在拉伸或按压后恢复原状的能力。就像一根高质量的橡皮筋,年轻的皮肤富含结构完整、功能良好的弹性蛋白纤维。然而,光老化的一个典型特征就是弹性纤维的变性降解,形成所谓的“弹性组织变性”,导致皮肤失去回弹力,变得松弛下垂。
而糖胺聚糖与透明质酸都是皮肤的“蓄水池”。糖胺聚糖(GAGs)是高度亲水的长链多糖,它们能与蛋白质结合形成蛋白聚糖。其中最著名的是透明质酸(玻尿酸),它能够吸收自身重量1000倍以上的水分,在皮肤真皮层形成巨大的水合凝胶,维持组织的饱满度和湿润度。这种“水库”效应对于皮肤容积的维持至关重要,其流失直接导致皮肤干燥、凹陷和细纹的产生。
健康的ECM依赖于合成与降解之间的精细平衡。这一过程主要由一系列酶精准调控,其中最关键的是基质金属蛋白酶(MMPs)。MMPs能够降解胶原蛋白、弹性蛋白等多种ECM成分。在正常生理状态下,MMPs的活性被其抑制剂(TIMPs)所平衡,同时,新的ECM成分由成纤维细胞不断合成,以替代被降解的旧成分,从而实现ECM的良性周转。然而,在衰老过程中,这种平衡被打破,导致了ECM的净损失。


细胞外基质的退化是一个多因素驱动的过程,内在的遗传编程和外在的环境侵蚀共同作用,加速了其崩塌。
内在衰老是由遗传因素决定的、普遍发生的生理性衰退过程,也是不可抗拒的生理时钟,具体表现在:
成纤维细胞功能衰退。随着年龄增长,真皮中的成纤维细胞数量减少,其合成胶原蛋白、弹性蛋白和GAGs的能力也显著下降。这些细胞本身也会进入衰老状态,分泌一系列破坏性因子(SASP),进一步加剧ECM的降解。
激素水平变化。特别是女性在绝经后,雌激素水平急剧下降。雌激素能促进胶原蛋白合成、抑制其降解,并增加皮肤透明质酸含量。因此,雌激素的减少是导致女性皮肤在更年期后迅速变薄、出现皱纹的重要原因之一。
而外源性衰老主要源于环境因素,其中紫外线辐射是最主要的元凶,这一过程又被称为“光老化”,例如:
紫外线(UV)辐射:UV,特别是长波紫外线(UVA)和中波紫外线(UVB),是破坏ECM的最强外部因素。UV照射能直接损伤成纤维细胞的DNA,并诱导皮肤产生大量的活性氧(ROS),引发氧化应激。ROS不仅直接降解胶原蛋白等ECM成分,更重要的是,它能激活一系列细胞信号通路(如AP-1、NF-κB),导致MMPs(如胶原降解关键酶MMP-1)的表达急剧上调,同时抑制I型前胶原的合成。研究表明,仅一次最小红斑量的UV照射,就足以在数小时内使皮肤中MMP-1的水平显著升高。这种持续的、失衡的MMPs高表达,是光老化皮肤中胶原蛋白大量流失的核心机制。
糖化反应:当饮食中过量的糖分与皮肤中的胶原蛋白、弹性蛋白等结合时,会通过非酶糖基化反应形成晚期糖基化终末产物(AGEs)。AGEs会使原本柔韧的蛋白质纤维变得僵硬、脆弱、易断裂,并呈黄褐色。这个过程就像在皮肤中发生了“美拉德反应”,使ECM失去弹性,皮肤变得暗黄、僵硬,更容易产生皱纹。
环境污染与吸烟:空气中的颗粒物(PM2.5)和烟草烟雾中的化学物质同样能诱导氧化应激和炎症反应,激活MMPs,加速ECM的降解。
面部表情与重力:重复的面部表情肌肉收缩会反复折叠皮肤,久而久之在ECM脆弱的区域形成静态纹。重力则持续地将组织向下拉,加剧了皮肤松弛和下垂。
营养与生活方式:营养不良(如维生素C缺乏,它是胶原合成必需的辅因子)、长期睡眠不足、慢性压力等,都会通过影响成纤维细胞功能或加剧氧化应激,间接损害ECM健康。

对抗皮肤衰老,核心策略在于保护现有的ECM免遭破坏,并刺激新的健康ECM合成。
1.防护至上:筑起抵御外敌的“长城”
严格防晒:这是保护ECM性价比最高、最有效的措施。应坚持每日使用广谱防晒霜(防护UVA和UVB,SPF30+/PA+++以上),并结合物理防晒(帽子、太阳镜等)。这能直接阻断UV诱导的MMPs激活和氧化损伤。
抗氧化防御:在护肤品中使用抗氧化剂,可以帮助中和ROS,减轻氧化应激对ECM的破坏。已被广泛研究的成分包括:
维生素C(L-抗坏血酸):强大的抗氧化剂,同时是胶原蛋白合成必需的辅因子,还能抑制MMP-1的活性。
维生素E(生育酚):与维生素C有协同抗氧化作用。
阿魏酸:与维生素C和E联用,能显著提升其光稳定性及抗氧化能力。
其他:如白藜芦醇、艾地苯醌、麦角硫因等。
2. 刺激再生,赋能成纤维细胞,重建ECM
维A类及其衍生物:视黄醇(维生素A)是迄今为止被临床研究证实最有效的抗衰老成分之一。它能够通过激活细胞核内的特定受体,促进成纤维细胞合成I型和III型胶原蛋白,抑制胶原降解,并改善因光老化导致的色素不均和粗糙纹理。
胜肽:一些胜肽能够作为信号分子,模拟ECM片段或生长因子的功能,刺激胶原蛋白的合成。例如,棕榈酰五肽-4、乙酰基六肽-8等。
生长因子:如表皮生长因子(EGF)、成纤维细胞生长因子(FGF)等,它们能直接促进细胞增殖与分化,刺激ECM的合成。常见于高端护肤品和再生医学领域。
3. 对抗糖化与抗炎
抗糖化成分:如肌肽,它能牺牲自身与糖结合,保护蛋白质免受糖化;此外,一些植物提取物如合欢树皮提取物也被报道具有抗糖化作用。
抗炎与屏障修护:维持皮肤屏障健康,使用含神经酰胺、积雪草提取物等成分的护肤品,可以减少低度炎症,为ECM的健康提供一个稳定的内部环境。
4. 生活方式与营养支持
均衡饮食:摄入富含抗氧化剂的食物(如多彩蔬菜水果)、优质蛋白质(胶原蛋白合成的原料)、以及富含Omega-3脂肪酸的食物(抗炎)。同时,控制精制糖的摄入,以减缓糖化反应。
补充胶原蛋白肽:一些研究表明,口服特定分子量的胶原蛋白肽后,其消化产物(寡肽)可能被吸收并定向到达皮肤,刺激成纤维细胞合成更多的胶原蛋白,改善皮肤弹性和水分。
戒烟限酒、保证睡眠、管理压力:这些措施能全面降低身体的氧化应激和炎症水平,对维持ECM健康至关重要。
5. 专业医美干预
当护肤品效果有限时,医美手段可以直接作用于真皮层,更强力地刺激ECM重塑。
激光与射频:如点阵激光、热玛吉等。其原理是通过可控的热损伤,激发创伤后修复反应,大量招募成纤维细胞并刺激其合成新的、排列更整齐的胶原蛋白。
微针:通过物理穿刺在皮肤上制造微孔,既能直接刺激胶原再生,也为透皮给予生长因子等活性成分提供了通道。
注射填充:如透明质酸填充剂,可以直接补充真皮流失的容积,立竿见影地改善皱纹和凹陷。一些刺激胶原新生的产品如聚左旋乳酸(PLLA),也能长效地改善肤质和容积。


皮肤的衰老,本质上是一场发生在细胞外基质层面的“支撑结构危机”。胶原蛋白的流失、弹性蛋白的变性、透明质酸的减少,共同导致了皮肤的塌陷与松弛。幸运的是,科学的发展让我们不再只是这场危机的被动旁观者。
通过日复一日的严格防晒与抗氧化,我们能为ECM筑起坚固的防线;通过选择含有视黄醇、胜肽等有效成分的护肤品,我们能温和地激励ECM的自我更新;而借助先进的医美技术,我们更能发起强有力的“重建工程”。这一切努力,结合健康的生活方式,都指向同一个目标:延缓ECM的崩塌,甚至在一定程度上逆转它,从而长久地守护皮肤的紧致、弹润与光彩。
理解细胞外基质的秘密,意味着我们掌握了对抗皮肤衰老的更根本、更科学的武器。下一次,当您涂抹防晒霜或选择一款抗老精华时,希望您能想到,您正在为您皮肤深层的“青春脚手架”提供至关重要的支持。
参考文献及出处:
[1] Khavkin, J., & Ellis, D. A. (2011). Aging skin: histology, physiology, and pathology. Facial Plastic Surgery Clinics of North America, 19(2), 229-234.
[2] Rittié, L., & Fisher, G. J. (2015). Natural and sun-induced aging of human skin. Cold Spring Harbor Perspectives in Medicine, 5(1), a015370.
[3] Ganceviciene, R., Liakou, A. I., Theodoridis, A., Makrantonaki, E., & Zouboulis, C. C. (2012). Skin anti-aging strategies. Dermato-endocrinology, 4(3), 308–319.
[4] Varani, J., Dame, M. K., Rittie, L., Fligiel, S. E., Kang, S., Fisher, G. J., & Voorhees, J. J. (2006). Decreased collagen production in chronologically aged skin: roles of age-dependent alteration in fibroblast function and defective mechanical stimulation. The American Journal of Pathology, 168(6), 1861–1868.
[5] Uitto J. (2008). The role of elastin and collagen in cutaneous aging: intrinsic aging versus photoexposure. Journal of Drugs in Dermatology, 7(2 Suppl), s12–s16.
[6] Papakonstantinou, E., Roth, M., & Karakiulakis, G. (2012). Hyaluronic acid: A key molecule in skin aging. Dermato-endocrinology, 4(3), 253–258.
[7] Pittayapruek, P., Meephansan, J., Prapapan, O., Komine, M., & Ohtsuki, M. (2016). Role of matrix metalloproteinases in photoaging and photocarcinogenesis. International Journal of Molecular Sciences, 17(6), 868.
[8] Waldera, L., & Klette, E. (2019). Cellular senescence in skin aging and cancer. Experimental Dermatology, 28(6), 667-671.
[9] Brincat, M. P. (2000). Hormone replacement therapy and the skin. Maturitas, 35(2), 107–117.
[10] Fisher, G. J., Wang, Z. Q., Datta, S. C., Varani, J., Kang, S., & Voorhees, J. J. (1997). Pathophysiology of premature skin aging induced by ultraviolet light. The New England Journal of Medicine, 337(20), 1419–1428.
[11] Gkogkolou, P., & Böhm, M. (2012). Advanced glycation end products: Key players in skin aging?. Dermato-endocrinology, 4(3), 259–270.
[12] Krutmann, J., Bouloc, A., Sore, G., Bernard, B. A., & Passeron, T. (2017). The skin aging exposure. Journal of Dermatological Science, 85(3), 152–161.
[13] Hughes, M. C., Williams, G. M., Baker, P., & Green, A. C. (2013). Sunscreen and prevention of skin aging: a randomized trial. Annals of Internal Medicine, 158(11), 781–790.
[14] Nusgens, B. V., Humbert, P., Rougier, A., Colige, A. C., Haftek, M., Lambert, C. A., ... & Lapière, C. M. (2001). Topically applied vitamin C enhances the mRNA level of collagens I and III, their processing enzymes and tissue inhibitor of matrix metalloproteinase 1 in the human dermis. Journal of Investigative Dermatology, 116(6), 853–859.
[15] Kong, R., Cui, Y., Fisher, G. J., Wang, X., Chen, Y., Schneider, L. M., & Majmudar, G. (2016). A comparative study of the effects of retinol and retinoic acid on histological, molecular, and clinical properties of human skin. Journal of Cosmetic Dermatology, 15(1), 49–57.
[16] Zhang, L., & Falla, T. J. (2009). Cosmeceuticals and peptides. Clinics in Dermatology, 27(5), 485–494.
[17] Mehta, R. C., & Fitzpatrick, R. E. (2007). Endogenous growth factors as cosmeceuticals. Dermatologic Therapy, 20(5), 350–359.
[18] Schagen, S. K., Zampeli, V. A., Makrantonaki, E., & Zouboulis, C. C. (2012). Discovering the link between nutrition and skin aging. Dermato-endocrinology, 4(3), 298–307.
[19] Choi, F. D., Sung, C. T., Juhasz, M. L., & Mesinkovsk, N. A. (2019). Oral Collagen Supplementation: A Systematic Review of Dermatological Applications. Journal of Drugs in Dermatology, 18(1), 9-16.
[20] Alexiades-Armenakas, M. R., Dover, J. S., & Arndt, K. A. (2008). The spectrum of laser skin resurfacing: nonablative, fractional, and ablative laser resurfacing. Journal of the American Academy of Dermatology, 58(5), 719–737.
本文由山东大学齐鲁医学院教授、博士生导师郝爱军复核。Bioπ中国美肤科学传播平台发布本文只是为了更多的信息参考,不代表任何有倾向性的投资意见或市场暗示。
THE END

京公网安备11010502058609号






















