科学公报
Nature:皮肤研究的五大亮点
2025年09月22日 14:50


涂有活体皮肤的机器人看起来更人性化,也许更具有亲和力。此外,皮肤的生物学特性——尤其是其自我修复能力——可以使此类涂层比合成涂层更耐用。然而,一个重要的挑战是找到一种将皮肤牢固地附着在机器人表面的方法。东京大学的一个团队设计了一种受天然皮肤韧带启发的潜在解决方案。
该小组由工程师 Michio Kawai 领导,此前曾在模拟皮肤中涂覆过机械手指——一种生物材料,由胶原蛋白和人类真皮成纤维细胞组成的真皮内层,以及由胶原蛋白和角质形成细胞形成的表皮组成。但这些层以液体形式应用,然后凝固,并没有牢固地附着在机械手指上。
为了解决这个问题,Kawai 的团队将目光投向了皮肤韧带——真皮发送到更深层皮下组织以附着在身体上的柱状延伸。为了模仿这些,研究人员在要覆盖的材料上制作了 V 形管状孔。每个 V 的点都在材料的深处,两个尖端向表面开放。合成皮肤——胶原蛋白和成纤维细胞的溶液——被倒在管子上并流入管子中。该技术在皮肤的下侧形成钩状延伸,将其附着在表面上。
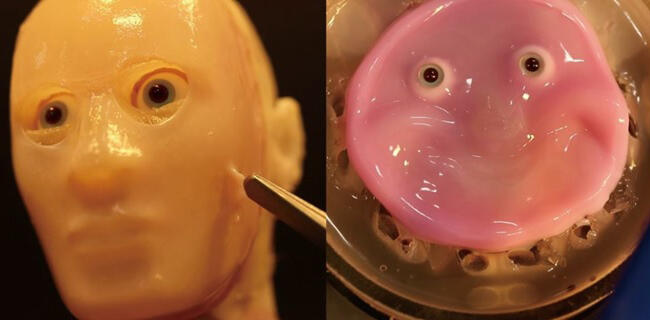
作者认为,如果人形机器人要作为社交伴侣发挥良好的作用,它们应该能够产生人类的表情。为此,Kawai 及其同事用韧带附着的真皮涂覆了面部模型,并在这个复杂的 3D 形状上长出一层表皮层。他们表明,通过有策略地将合成皮肤钩在嘴巴模型上,皮肤可以保持完整和柔韧,并在嘴巴形成微笑时随着模型脸颊的上升而移动。研究人员推测,通过培养皮肤下的肌肉纤维,可以实现更逼真的表情。

中毒性表皮坏死松解症(TEN)是一种严重的皮肤病,通常由药物不良反应引起。它杀死角质形成细胞,导致表皮脱落并导致大面积起泡。每年只有大约百万分之一的人会患上十,但大约 15% 的受影响者会死于此。没有有效的治疗方法。

蒂埃里・诺德曼(Thierry Nordmann )
蒂埃里・诺德曼(Thierry Nordmann,MD-PhD )是一位在皮肤研究领域有所建树的科研工作者。他的研究方向是皮肤的分子与空间生物学 ,就职于德国慕尼黑马克斯・普朗克生物化学研究所。德国马丁斯里德马克斯普朗克生物化学研究所的皮肤生物学家蒂埃里·诺德曼 (Thierry Nordmann) 领导的一项研究提供了一种潜在的治疗方法。该团队发现了驱动 TEN 的分子途径,并表明用现有药物阻断它可能会治疗这种疾病。
研究人员从对药物有过 TEN 或较轻微皮肤反应的人身上采集了皮肤样本,然后使用一种称为深度视觉蛋白质组学的技术对角质形成细胞和局部免疫细胞中的数千种蛋白质进行分类。TEN 诱导的变化包括称为 JAK/STAT 通路的细胞内信号网络中蛋白质的上调。激活该途径的干扰素和其他炎症信使也很丰富。角质形成细胞和免疫细胞都发生了变化,表明存在正反馈循环。
这些发现使作者认为抑制 JAK 酶的药物可能会阻止 TEN。小鼠模型中的测试证明了他们是正确的——JAK 抑制大大减少了动物的 TEN 皮肤损伤。

蒂埃里·诺德曼 (Thierry Nordmann) 获得2025 年 LEO 基金会奖
LEO 基金会是丹麦最大的商业基金会之一,也是利奥制药(LEO Pharma)的控股股东,此奖旨在表彰为皮肤研究做出杰出贡献的优秀年轻研究人员,每个奖项奖金为 10 万美元 。最后,该团队使用一种选择性阻断 JAK1 酶亚型的药物(一种已获准用于不同疾病的药物)在临床上测试了他们的假设。7 名患有 TEN 或稍轻的相关疾病的人接受了治疗;所有人都健康地离开了医院,没有出现副作用。

挠痒的感觉很好。但对于患有湿疹等慢性皮肤病的人来说,这种作用会加重皮炎,通常会引发抓挠越来越痒的皮肤的令人沮丧的循环。
为了确定瘙痒可能有什么好处,并探索这些好处背后的机制,宾夕法尼亚州匹兹堡大学的皮肤科医生 Andrew Liu 和他的同事检查了免疫细胞和感觉神经元之间的相互作用,这些相互作用将抓挠和炎症联系起来小鼠。他们发现抓挠可以增强对皮肤细菌感染的免疫反应。
Andrew Liu的团队专注于肥大细胞——在过敏反应和瘙痒中起核心作用的免疫细胞。研究人员表明,这些细胞与两类皮肤支配的感觉神经元相互作用,形成一个循环,将瘙痒与抓挠联系起来,然后与瘙痒加剧和抓挠加剧联系起来。

该研究使用各种引起瘙痒的分子来证明瘙痒敏感神经元的激活如何使动物抓挠受影响的皮肤。然后它展示了这种抓挠如何导致第二种神经元类型(通常与疼痛感相关)局部释放一种称为 P 物质的神经肽。该分子与驱动瘙痒感的抗体和其他信使相互作用,进一步激活肥大细胞。
最后,研究人员发现,在小鼠中,抓挠可以增强对皮肤细菌的免疫反应。它还减少了小鼠皮肤微生物组的局部多样性。当动物感染金黄色葡萄球菌时,抓挠会增加免疫反应。通过将抓挠反应的组成部分映射到瘙痒,该研究提出了减轻抓挠有害影响的目标。

皮肤是丰富多样的微生物的家园。免疫系统定期控制这种微生物群,以防止其破坏皮肤功能或引起全身感染。长期以来,人们一直认为这是通过循环产生抗体的 B 细胞、直接识别微生物的 T 细胞和在皮肤中巡逻的抗原呈递细胞的联合作用来实现的。所有这些细胞都被认为会移动到淋巴结,在那里它们相互作用并调节彼此的免疫功能。

因塔・格里博尼卡博士(Inta Gribonika, PhD)与其团队成员
但由位于马里兰州贝塞斯达的美国国立卫生研究院的免疫学家 Inta Gribonika 领导的一个团队发现,当小鼠的皮肤被以前从未遇到过的细菌定植时,皮肤本身就会产生自主免疫反应。通过将表皮葡萄球菌引入无病原体小鼠的皮肤中,Gribonika 和她的同事发现了一种局部抗体介导的免疫,表明某些 B 细胞是关键参与者。
研究小组接下来表明,这些 B 细胞被一组局部 T 细胞激活,这些 T 细胞从免疫抑制表型转变为促免疫表型。驻留在皮肤中的称为朗格汉斯细胞的专业抗原呈递细胞对于诱导这种免疫反应至关重要。研究发现,B 细胞、T 细胞和朗格汉斯细胞都在皮肤中相互作用,而不是像预期的那样在淋巴结中相互作用。以前被认为只有在炎症条件下才能形成的“三级”淋巴器官聚集在暴露于细菌的毛囊周围,以协调局部免疫反应。
研究人员表明,阻断皮肤的局部免疫反应会导致表皮链球菌皮肤种群不受控制的生长,并且这种基于皮肤的反应可以防止全身感染。在皮肤被表皮链球菌定植后表现出这种反应的小鼠在随后将这种细菌注射到血液或更深的皮肤层时对感染具有抵抗力。该研究表明,皮肤本身是抵御定植细菌的第一道防线,揭示了人体免疫系统的意想不到的因素。

未愈合的皮肤伤口——包括手术或外伤造成的伤口,以及糖尿病足溃疡和压疮——是一个巨大的医疗问题。医疗专业人员通常需要定期检查此类伤口,以确保并发症和感染得到快速处理。

吉列尔莫·阿米尔(Guillermo Ameer)(左图)
约翰·罗杰斯( John Rogers)(右图右一)
技术可以在临床环境之外实时跟踪伤口愈合和感染。由伊利诺伊州埃文斯顿西北大学的工程师吉列尔莫·阿米尔和约翰·罗杰斯领导的团队描述了一种小型可穿戴设备,该设备使用水蒸气、二氧化碳和挥发性有机化合物 (VOC) 的测量来监测愈合和细菌生长。
该无线设备大约有乐高积木那么大,重 11 克。将其凹面压在皮肤上形成一个小腔室,传感器在其中跟踪水蒸气浓度的变化,CO2以及从身体表面扩散的挥发性有机化合物。设备底座上的传感器测量皮肤温度、导热系数和电阻抗。



吉列尔莫·阿米尔和约翰·罗杰斯领导的团队开发的一种小型可穿戴设备
为了跟踪伤口愈合,该设备依赖于这样一个事实,即病变会破坏皮肤的屏障功能,从而允许更多的水逸出。随着愈合的进行,这种释放的速度会减弱。在对健康小鼠和 2 型糖尿病小鼠模型的测试中,该设备的水读数清楚地跟踪了伤口愈合,发现糖尿病动物的伤口愈合速度较慢。
该设备还可以检测感染。在小鼠中,受感染的伤口会产生可识别的挥发性有机化合物尖峰,这些挥发性有机化合物通常由细菌释放。当人类志愿者三天不清洗而让他们的皮肤微生物群积聚时,挥发性有机化合物飙升了近八倍。
研究人员报告说,该系统还可以跟踪进入皮肤的化学物质,从而可以监测接触环境毒素的情况。该设备可能过于笨重,无法持续监测足部溃疡或褥疮等情况。但这项研究可能标志着在追求持续、家庭监测伤口愈合方面迈出了关键一步。
本文转自www.nature.com,是《自然展望:皮肤》的一部分;文图版权归著作权人。必须说明的是,由于是机器自动翻译,不保证内容翻译的百分百准确性和严谨性,建议阅读原文。Bioπ中国美肤科学传播平台发布本文只是为了更多的信息参考,不代表任何有倾向性的投资意见或市场暗示。
THE END

京公网安备11010502058609号





















