谈糖不色变
燕窝酸的作用机理及其在修复过程中的作用
2026年01月13日 13:14

燕窝酸(主要形式为N-乙酰神经氨酸,Neu5Ac)是一种九碳酸性糖,主要位于糖蛋白和糖脂的末端,在细胞通讯和功能调节中发挥关键作用[1]。燕窝酸赋予细胞表面负电荷,被公认为一种抗黏附糖型。一个典型例子是红细胞,其表面高度燕窝酸化并带有负电荷。血管内皮的管腔表面同样富含燕窝酸残基,这种电荷排斥作用防止红细胞黏附,并使其能够在循环系统中自由无阻地通过[1]。
燕窝酸的作用机理主要包括:
• 细胞识别与信号传导:燕窝酸作为糖链末端残基,调节细胞间相互作用、黏附和信号传导。
○ 燕窝酸在神经发育中的作用:多聚燕窝酸(PSA)的添加是神经细胞粘附分子(NCAM)一种非常重要的翻译后修饰。PSA是由α2-8连接燕窝酸线性同聚物构成的大分子。在大脑中,PSA是燕窝酸与蛋白质结合的主要形式,超过95%的PSA都与NCAM结合。由于燕窝酸带负电荷,PSA-NCAM是神经细胞粘附分子(NCAM)中粘附性较弱的形式,保证了大脑发育过程中以及成熟期后突触的可塑性,影响神经元突起生长和记忆形成。[2]
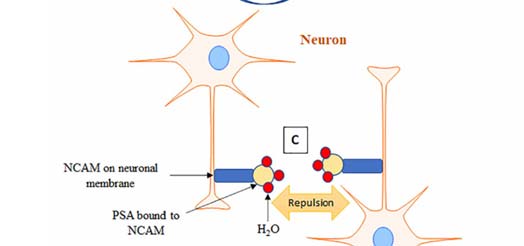
NCAM上的PSA会产生立体化学排斥,从而阻止相对细胞上NCAM分子之间的同亲性接触(homophilic contacts)
○ 燕窝酸在皮肤抗衰上的作用:成纤维细胞是维持皮肤稳态以及协调生理组织修复和皮肤再生的关键细胞。随着衰老和细胞衰老过程的发生,成纤维细胞功能障碍会导致老年人皮肤再生延迟。在TGF-β1刺激后,通过HAS2合成的透明质酸促进CD44向脂筏(lipid rafts)的重新定位;CD44与表皮生长因子受体(EGFR)的结合之后激活肌成纤维细胞分化所需的MAPK/ERK信号通路。在衰老的成纤维细胞中,燕窝酸酶NEU1表达增加,导致CD44去燕窝酸化,即使在TGF-β1刺激后,CD44也无法重新定位到脂筏。因此,CD44无法再与EGFR结合,导致肌成纤维细胞分化受到抑制。调控成纤维细胞中的燕窝酸化是一种新的策略,用于老年相关皮肤疾病的预防和再生治疗,以及用于美容护肤。[6]
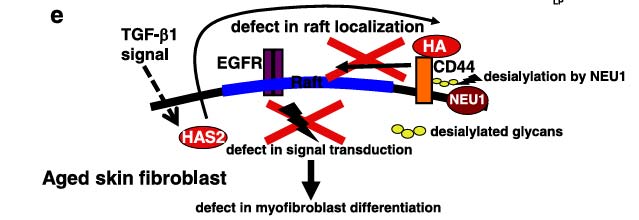
CD44燕窝酸化调控肌成纤维细胞分化
• 免疫调节:燕窝酸化在免疫系统中发挥多方面的作用。它通过与SIGLECs的相互作用,参与免疫应答。此外,抗体的燕窝酸化能够调节抗体的功能。
○ 燕窝酸与SIGLEC的结合:SIGLECs是一类主要表达于免疫细胞(如白细胞和巨噬细胞)的燕窝酸结合蛋白家族,已知可调控炎症信号。SIGLEC-1的燕窝酸化可诱导抗原的内化,通过将抗原呈递给树突状细胞(DCs)或B细胞,从而启动免疫应答。相反,SIGLEC-2、3以及5-11的燕窝酸化可通过调控Toll样受体信号抑制促炎信号,而SIGLEC-14、-15和-16被燕窝酸激活后则可通过MAPK和AKT信号通路刺激促炎反应。[1]
○ 燕窝酸与抗体的结合:人源免疫球蛋白G(IgG)主要含有α-2,6-连接的燕窝酸残基。IgG抗体Fc段N-糖链末端的燕窝酸修饰后,可以降低抗体依赖的细胞介导的细胞毒性(ADCC),表现出增强的抗炎特性。燕窝酸残基的负电荷可能改变了抗体分子的整体电荷,降低了其等电点并影响了抗原结合。[1]
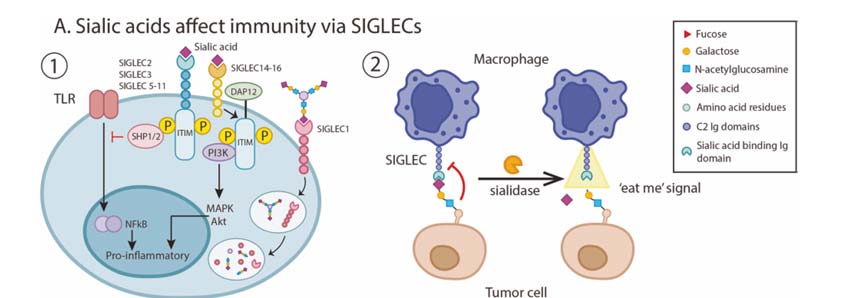
燕窝酸通过SIGLEC进行免疫调节
• 抗氧化与抗终末糖化:
○ 抗氧化:燕窝酸具有独特的α-酮酸结构,可以作为一种内源性抗氧化剂。已知组织和器官中仅存在极少量的游离单体燕窝酸,但作为燕窝酸糖蛋白(sialoglycoproteins)和燕窝酸糖脂(sialoglycolipids)的末端残基糖却非常丰富。末端燕窝酸残基可被神经氨酸酶去除,产生游离的燕窝酸分子,与等摩尔量的H₂O₂反应,发挥抵御氧化损伤的防御作用。此外,调控H₂O₂浓度的机制不仅对解毒至关重要,在信号转导中也同样重要,因为H₂O₂可作为第二信使。[3]
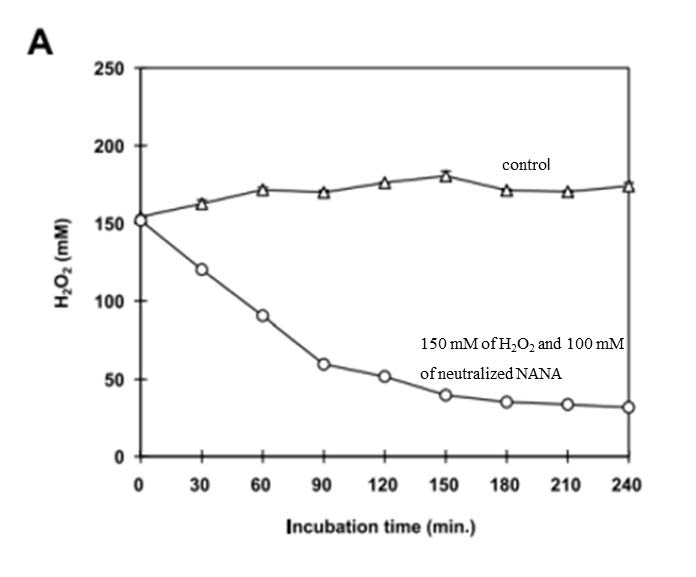
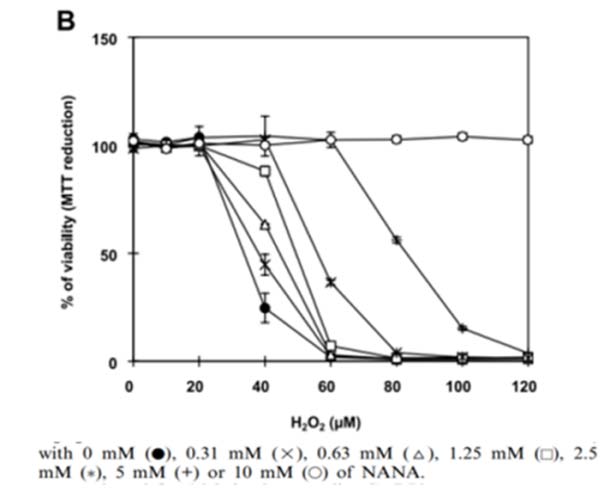
体外生化实验及细胞研究表明:燕窝酸能清除H₂O₂自由基,增加因H₂O₂氧化损伤细胞的存活率
○ 抗终末糖化:非酶促糖化反应产生的终末糖化产物(AGEs)可以改变细胞外基质(ECM)蛋白的结构和功能,例如胶原蛋白和弹性蛋白的糖基化反应导致纤维间形成交联,增加ECM的刚性而降低弹性。随着年龄增加和肌肤衰老,AGEs会逐渐积累 [4]。燕窝酸在人体中通常作为聚糖的远端修饰而存在,在生理条件下燕窝酸修饰能够给糖带上负电荷,从而影响其构象和寡聚,进而影响AGEs的生成。有研究探讨了燕窝酸对体外牛血清白蛋白(BSA)生成AGEs荧光的影响,发现燕窝酸能有效抑制葡萄糖和果糖诱导的BSA荧光增强 [5],表明燕窝酸具有潜在抑制非酶促糖化反应的能力。华熙内部的实验数据也表明,燕窝酸可以显著抑制AGE和AGE前体(Amadori产物和二羰基化合物)的产生,表现出很好的抗终末糖化的能力。
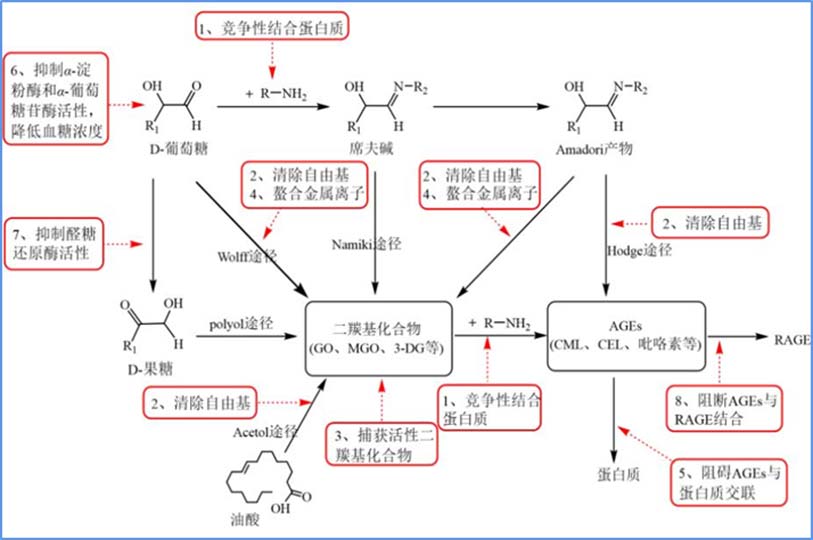
终末糖化(AGE)路径
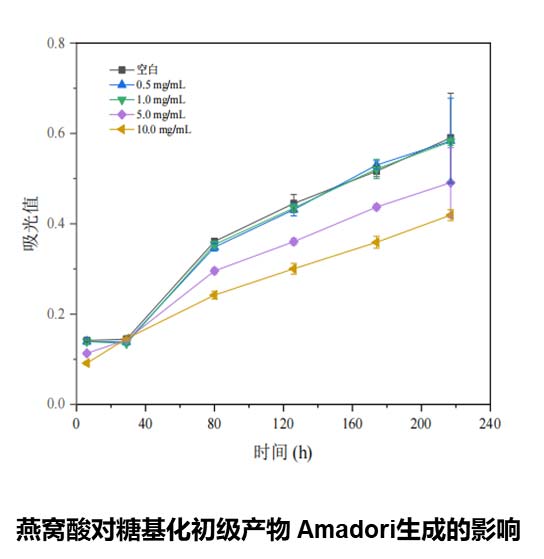
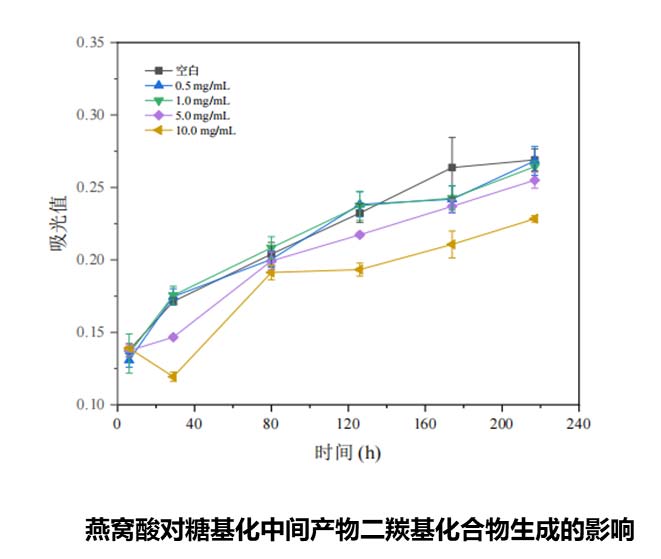
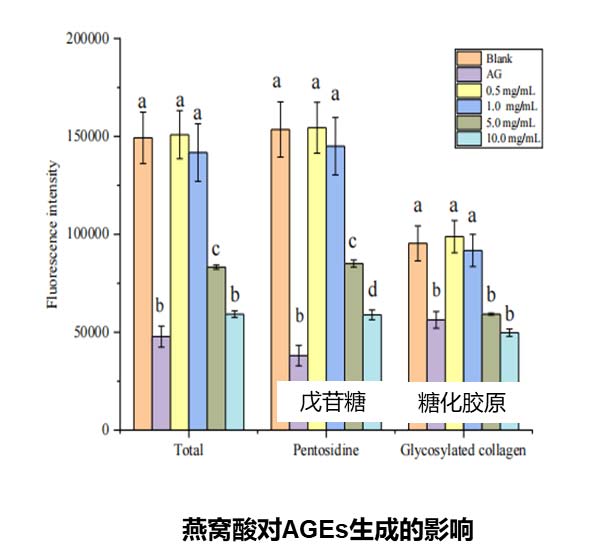
燕窝酸在修复过程中的作用:
• 神经修复:燕窝酸促进神经可塑性和修复,特别是PSA-NCAM在神经损伤后增强神经元再生、轴突迁移和突触重塑。局部PSA的过表达可以促进轴突再生和神经连接性。同样,表达PSA的Schwann细胞可增强损伤后Purkinje轴突的再生。[1]
• 皮肤修复:随着衰老,成纤维细胞中燕窝酸化的减少是老年相关病理的风险因素,引起老年人慢性伤口。调控成纤维细胞中的燕窝酸化是一种新的策略,可用于老年相关皮肤疾病的预防和再生治疗,以及用于美容护肤。
• 心血管修复:ApoB是极低密度脂蛋白和低密度脂蛋白(LDL)的主要成分,其含有燕窝酸化糖基化位点。心血管疾病患者血浆LDL水平升高,但其燕窝酸含量减少。这些低燕窝酸化LDL颗粒更容易被人体主动脉细胞摄取,导致细胞内胆固醇酯蓄积增加。动脉粥样硬化的小鼠模型实验显示,给予燕窝酸可减轻高脂血症小鼠的动脉粥样硬化,减少动脉粥样硬化斑块形成和肝脏脂质蓄积。[1]

婴幼儿大脑和骨骼快速生长对营养需求极高。比如燕窝酸是脑神经节苷脂(gangliosides)和PSA-NCAM的关键成分,可以促进神经元迁移、突触连接和记忆形成,对认知发育至关重要。
科学家发现,因遗传原因引起的NANS (燕窝酸合酶)基因突变,其编码燕窝酸合成酶无法表达,关键组织燕窝酸化缺乏,导致婴儿期大脑严重发育迟缓和骨骼发育不良。斑马鱼验证也发现,敲除斑马鱼胚胎中NANS基因,结果导致斑马鱼的骨骼发育异常,同时外源性补充SA可以部分恢复NANS缺失造成的生长表型。[7]
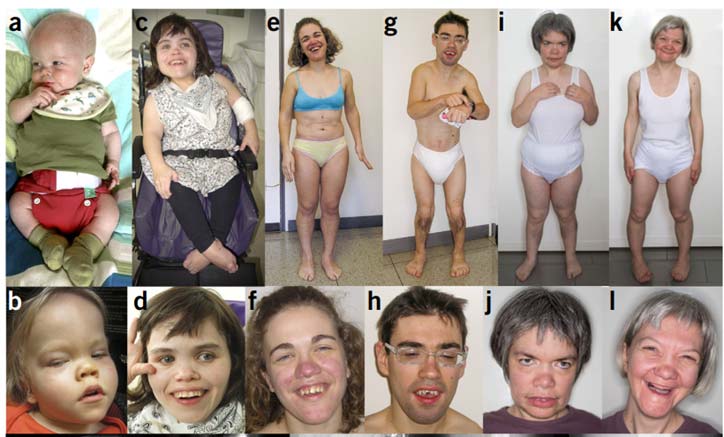
NANS缺陷症患者的形态学和骨骼特征
华熙内部实验也发现,小鼠出生后持续补充华熙燕窝酸6周,能显著增强记忆及认知能力,而且神经细胞黏附因子(NCAM)水平也得到了提升。
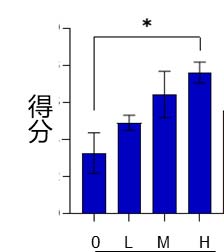
Y迷宫实验
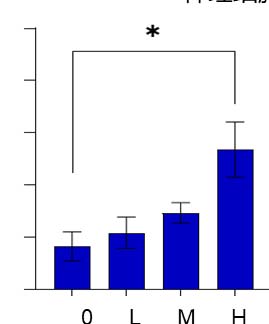
NCAM1水平
其他研究还发现,孕期补充燕窝酸对于婴幼儿的发育也可能有很大影响。从妊娠第15天到出生后第 21 天,对母鼠进行燕窝酸和水灌胃给药。之后测试100日龄的子代鼠在Morris水迷宫表现,同时检测子代大脑皮层海马体中燕窝酸的含量。研究发现,大鼠母体孕期补充燕窝酸能有效促进子代脑内燕窝酸含量的增加,同时增强其认知能力。[8]
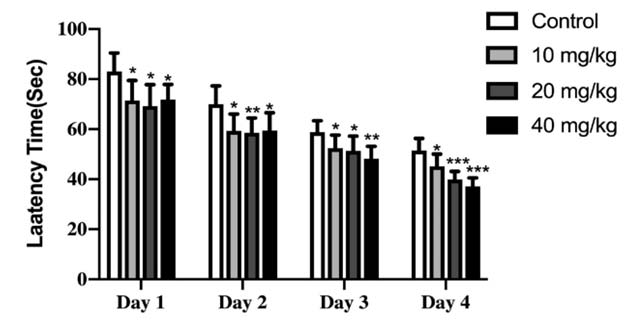
100日龄雄性大鼠在Morris水迷宫试验中找到平台的潜伏期
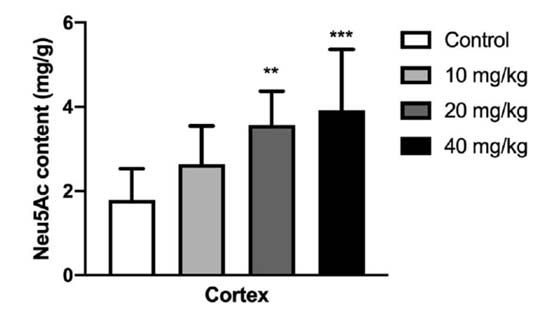
100日龄雄性大鼠大脑皮层燕窝酸含量

糖基化是一系列酶促反应,在这些反应中,碳水化合物被附着到蛋白质或脂质上,通常称为“糖链”(glycans)。蛋白质糖基化是最常见的二级修饰之一,不同糖链延伸的添加会极大地影响糖蛋白的结构和功能。糖链与蛋白质序列不同,蛋白质序列由基因决定,而糖链没有遗传模板。相反,糖基化由众多基因及其产物控制,这些基因在复杂的网络中相互作用,并进一步受到表观遗传修饰和环境的影响。由于糖基化随衰老呈现可预测的变化模式,这促使科学家开发了完全基于附着在蛋白上糖链的“糖链时钟”。糖链时钟的加速与多种与炎症和代谢健康不良相关的生化和生理特征相关,这些特征反映了生物衰老。由于糖链对环境刺激的高度可塑性,使糖链时钟成为预测生物年龄的最佳指标之一。新研究还显示,通过简单的生活方式改变(如减重、膳食补充剂和运动),以及医疗干预(如减重手术和性激素调节),糖链时钟有可能被逆转。[10]
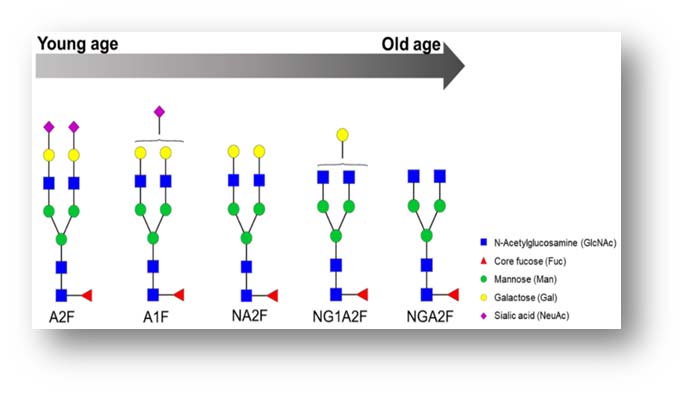
燕窝酸化是糖基化的关键一环,是糖链的末端修饰。燕窝酸化的减少和半乳糖的暴露增加和与年龄相关的疾病以及人类衰老有关。研究发现α2-3燕窝酸化的O-聚糖的数量随着细胞衰老而减少,胚胎来源的细胞的α2-6和α2-3燕窝酸化的N-聚糖和O-聚糖的总体信号也明显强于衰老的细胞。该现象一致地呈现在成纤维细胞和各种其他细胞类型中。随着人类衰老,去燕窝酸化的衰老细胞在体内逐渐积累,对信号转导和分子识别等生物功能产生不利影响。体现在功能上,早期和晚期传代的成纤维细胞的细胞迁移能力不同,衰老的人类皮肤成纤维细胞的迁移明显减少。由此可见,衰老细胞的燕窝酸化干预对生物衰老干预很重要[9]。
P21 是细胞周期蛋白依赖性激酶(CDK)抑制剂,通常在衰老细胞中积累,阻断细胞周期进程,通常作为衰老细胞的标记。P53在衰老的细胞中积累,是细胞周期蛋白的关键调节因子。华熙内部的实验数据发现用燕窝酸处理,可以显著逆转成纤维细胞的衰老,P21和P53的表达都明显下降,使得衰老细胞的I型和III型胶原的表达也得到明显恢复。在3D衰老皮肤组织中,经过燕窝酸的处理,皮肤组织的I型胶原蛋白生成显著增加,表皮的厚度也得到了提升,皮肤组织形态也变得更好。这些实验结果均表明,糖链时钟对应的生物衰老是可以干预的,且有可能被逆转的。
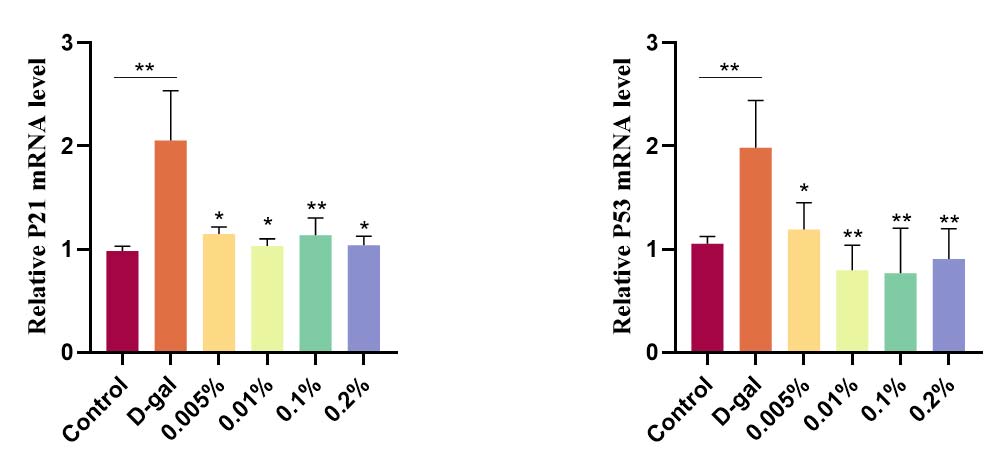
P21和P53在成纤维细胞中的表达
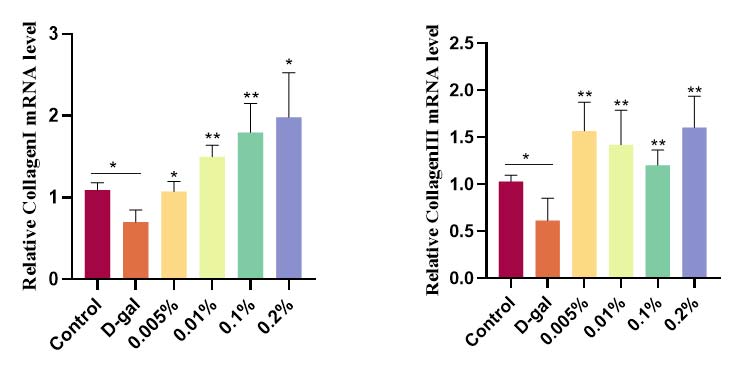
成纤维细胞的胶原1和3的表达
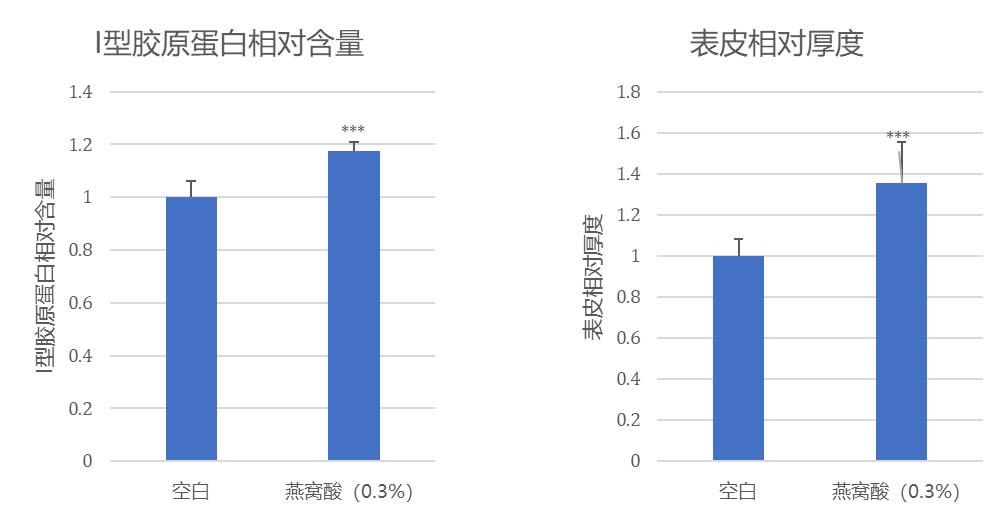
3D皮肤组织的I型胶原蛋白含量和表皮厚度
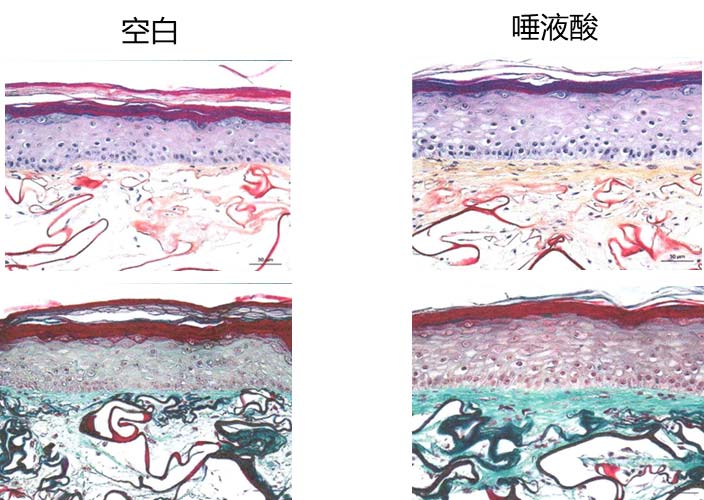
3D皮肤组织中的胶原纤维(黄色和绿色区域)和皮肤组织形态
参考文献
1,https://doi.org/10.1038/s41420-024-02180-3
2,https://doi.org/10.3389/fnins.2021.648617
3,https://doi.org/10.1016/s0014-5793(04)00164-4
4,https://doi.org/10.3181/00379727-196-43158c
5, https://doi.org/10.1007/bf00570371
6,https://link.springer.com/content/pdf/10.1186/s13287-017-0534-1.pdf
7,https://doi.org/10.1038/ng.3578
8,https://doi.org/10.3389/fnut.2021.641027
9,https://doi.org/10.1186/s13578-016-0079-5
10,https://doi.org//10.3389%2Ffcell.2022.982609
本文作者为孙欣博士。Bioπ发布本文只是为了传递更多的讯息,不代表任何有倾向性的投资意见或市场暗示,仅供参考。
THE END

京公网安备11010502058609号






















