科学公报
细胞外基质:
线粒体健康与免疫防御的隐秘守护者
2025年09月24日 14:48

细胞外基质(ECM)长期以来被视为细胞的支持性支架,而线粒体则是细胞的能量工厂,两者似乎互不关联。然而,近期发表于《Cell》的一项突破性研究揭示,ECM通过一种前所未有的机制,直接调控线粒体稳态与免疫功能。该研究发现了由透明质酸酶TMEM2介导的ECM重塑如何通过TGF-β信号通路精确控制线粒体,并最终影响机体的免疫防御能力。这一发现不仅重新定义了ECM的生物学功能,也为理解多种疾病的机制提供了全新视角。

研究人员通过构建TMEM2过表达(OE)和敲除(KO)细胞模型,证实TMEM2作为细胞表面透明质酸酶,可有效降解ECM中的透明质酸(HA)。功能实验显示,TMEM2-OE细胞对多种线粒体应激源(如鱼藤酮、无糖培养基)异常敏感,而TMEM2-KO细胞则表现出显著抵抗性。外源添加透明质酸酶可模拟TMEM2-OE表型,证明HA降解是导致线粒体应激敏感的直接原因。
进一步分析表明,TMEM2-OE直接损害线粒体功能:基础呼吸和最大呼吸能力下降,线粒体活性氧(ROS)水平升高。超分辨率显微镜观察发现,TMEM2-OE导致线粒体从正常管状网络断裂成碎片化点状结构,而TMEM2-KO细胞中线粒体网络更加连贯(图1)。这些变化并非由于线粒体数量或整体能量状态改变,而是功能特异性损伤。
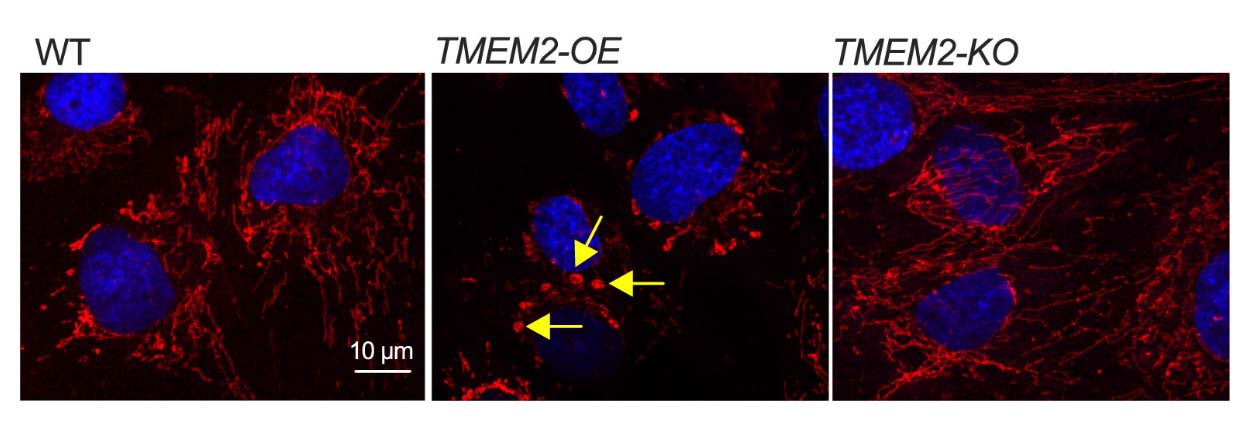
图1:通过超分辨率显微镜成像技术,直观地展示了不同细胞中线粒体的形态差异。

为验证这一机制的普适性,研究者在秀丽隐杆线虫中过表达人源TMEM2(hTMEM2)。结果显示,hTMEM2-OE同样激活了线虫的线粒体未折叠蛋白反应(UPRMT),且该过程依赖于转录因子ATFS-1。值得注意的是,线虫ECM主要成分类似HA的软骨素,hTMEM2-OE可有效降解软骨素并诱导UPRMT,其表型与过表达线虫自身软骨素酶基因CHHY-1一致。
hTMEM2-OE引起的线粒体碎片化和呼吸功能受损具有年龄依赖性,在年老线虫中尤为显著(图2)。利用 gst-4p::GFP(其表达依赖于转录因子SKN-1,即NRF2的同源物)和 cysl-2p::Venus(其表达依赖于HIF-1)进行检测。结果表明野生型hTMEM2 能诱导gst-4表达,hTMEM2(ED) 则不能(图3左)。当利用RNA干扰敲低SKN-1后,野生型hTMEM2诱导gst-4表达下调,证明是SKN-1依赖性的(图3右)。hTMEM2-OE不能有效激活HIF-1。说明hTMEM2诱发的应激反应是通路特异性的,它特异性地激活了抗氧化应激(SKN-1/NRF2)通路,而非低氧(HIF-1)通路。这再次证明其效应不是普通的细胞毒性,而是精确的信号传导。
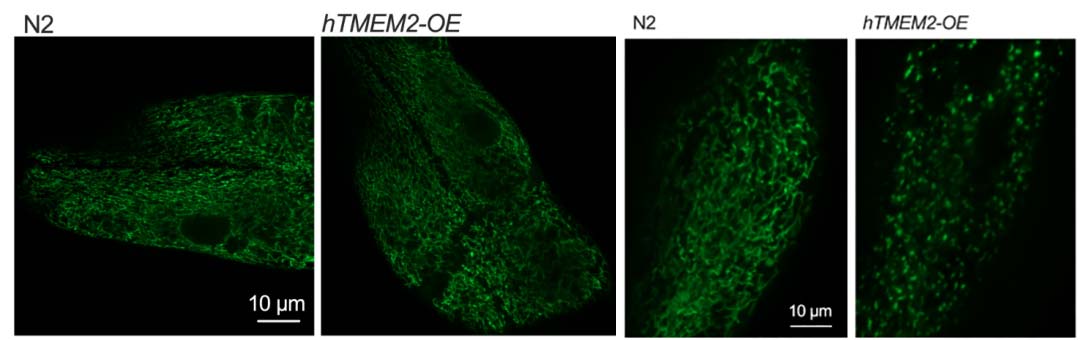
图2:年轻成虫中hTMEM2-OE线粒体形态变化(图2左侧);年老线虫中hTMEM2-OE线粒体碎片化(图2右侧)
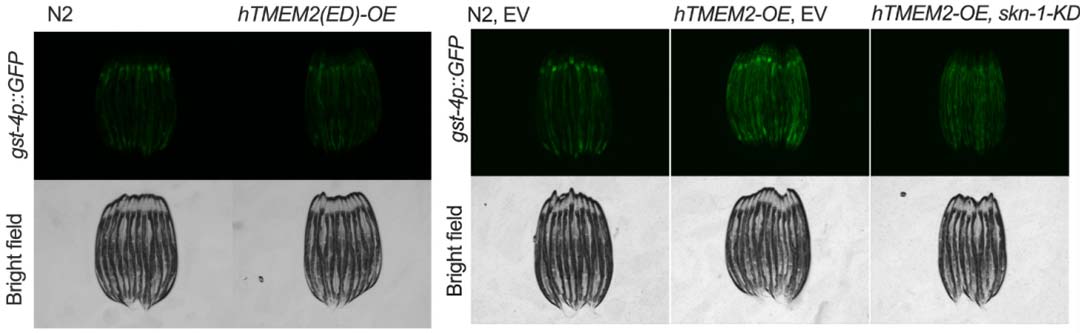
图3: hTMEM2 与hTMEM2(ED) 诱导gst-4表达不同(图2左侧);利用RNA干扰敲低 skn-1 后,野生型hTMEM2诱导gst-4表达下调(图2右侧)

为了找到介导这一通讯过程的关键膜蛋白,研究者在Cas9表达的野生型(WT)和TMEM2-OE细胞中,转导了一个靶向2073个质膜定位蛋白基因的sgRNA文库。然后用TMEM2-OE细胞敏感的鱼藤酮和无糖培养基进行筛选(图4)。理论上,任何能挽救TMEM2-OE细胞应激敏感性的基因敲除,其编码的蛋白都可能是该信号通路的一部分。结果显示在众多的“命中基因”中,最引人注目的是TGF-β受体(TGFBR)的两个亚基:TGFBR1和TGFBR2。它们的KO显著增强了TMEM2-OE细胞在应激下的生长能力。
在TMEM2-OE细胞中单独敲除TGFBR1或TGFBR2,足以有效挽救TMEM2-OE细胞在线粒体应激(CF培养基)下的生长缺陷(图5左)。这表明抑制TGF-β通路可以逆转ECM重塑带来的负面效应。使用TGFBR1的化学抑制剂SB431542处理TMEM2-OE细胞,得到了与基因敲除相同的效果——细胞对鱼藤酮的敏感性降低(图5中)。这进一步证实了TGF-β受体激酶活性在该过程中的必要性。对WT、TMEM2-OE和TGFBR1-KO TMEM2-OE细胞进行RNA测序发现,TMEM2-OE诱导的绝大部分转录组变化(约64%的上调基因和54%的下调基因)在TGFBR1被KO后发生了逆转(图5右)。这证明TGF-β信号通路是TMEM2-OE下游最主要的转录调控驱动器。研究还排除了整合素-FAK和经典透明质酸结合蛋白(如CD44)的参与,确证TGF-β通路的核心地位。
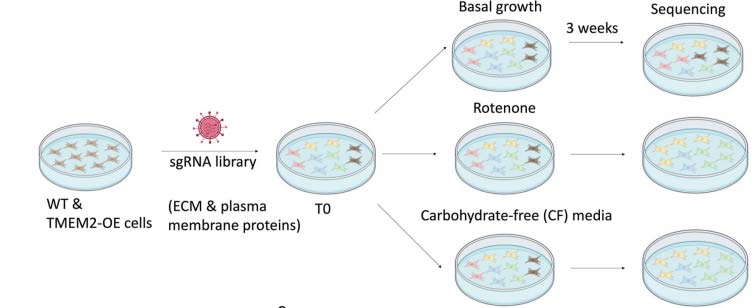
图4: 稳定表达Cas9的野生型(WT)或TMEM2过表达(TMEM2-OE)细胞经sgRNA文库转导后,在基础培养条件或线粒体应激条件下进行为期三周的筛选,随后进行测序分析
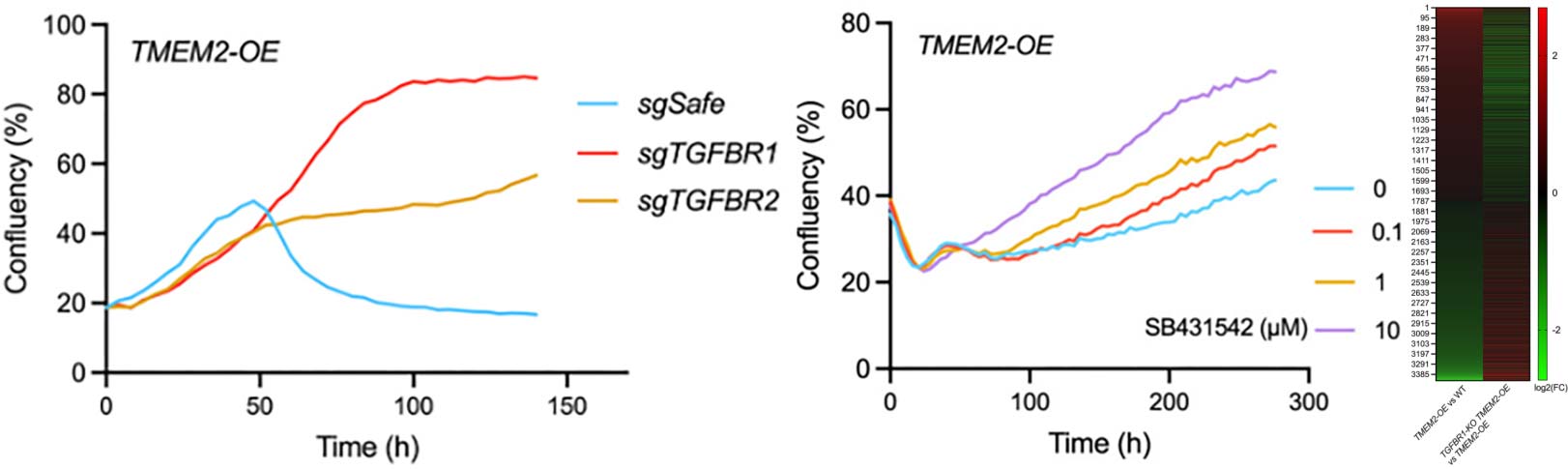
图5:证明TGF-β信号通路是TMEM2-OE下游最主要的转录调控驱动器

本研究还明确了TGF-β-SMAD信号通路是连接细胞外基质(ECM)重塑与线粒体功能紊乱的核心桥梁。研究人员首先从TGF-β家族中鉴定出TGF-β1和TGF-β2是关键配体,其外源添加可完美模拟TMEM2过表达诱导的线粒体应激敏感表型。机制上,完整的ECM通过高分子量透明质酸(HMW HA)抑制TGF-β信号,而TMEM2对HA的降解则解除这一抑制,进而激活经典的TGFBR-SMAD2/3/4信号轴。进一步研究发现,该通路是响应多种ECM紊乱(包括HA降解和弹性蛋白组装缺陷)的通用传感器。值得注意的是,这一从ECM到线粒体的通讯机制在进化上高度保守,线虫研究证实哪些TGF-β通路组分是hTMEM2诱导线粒体应激所必需的。结果说明TGF-β-SMAD信号通路在从线虫到人类的进化过程中高度保守,它同样介导了线虫中hTMEM2引发的线粒体应激反应。
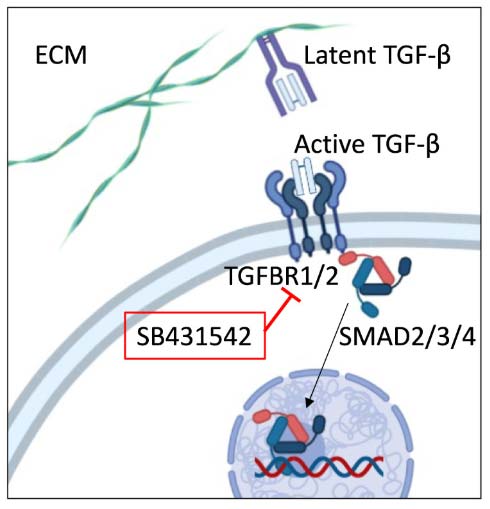
图6:TGF-β-SMAD通路直接调控线粒体分裂
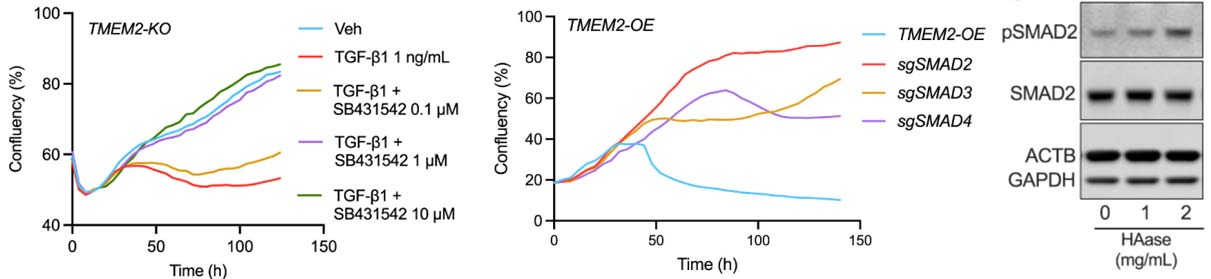
图7:证实信号通过经典的TGFBR-SMAD通路传导

外源TGF-β1处理可完美模拟TMEM2-OE表型,诱导线粒体碎片化和功能损害。RNA-seq分析发现,TGF-β1显著上调多种线粒体分裂基因(如DRP1、MTFP1、RALA),同时下调抗氧化基因。
最关键的是,使用线粒体分裂抑制剂(P110或Mdivi-1)可显著改善TMEM2-OE细胞的线粒体形态、呼吸功能及应激抵抗能力。这证明线粒体过度分裂是TMEM2-TGF-β通路导致功能损害的必要环节,确立了"ECM重塑→TGF-β激活→分裂基因上调→线粒体过度分裂→功能紊乱"的因果关系链。
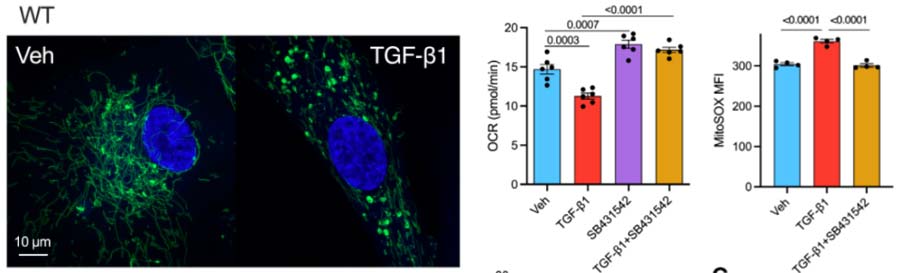
图8:TGF-β1诱导线粒体分裂和功能紊乱
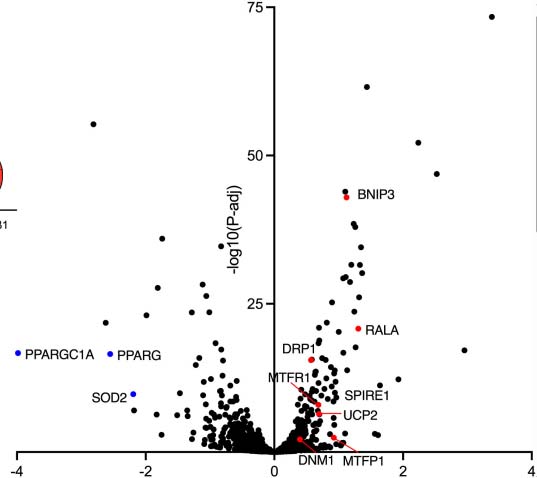
图9:TGF-β1对线粒体相关基因表达调控
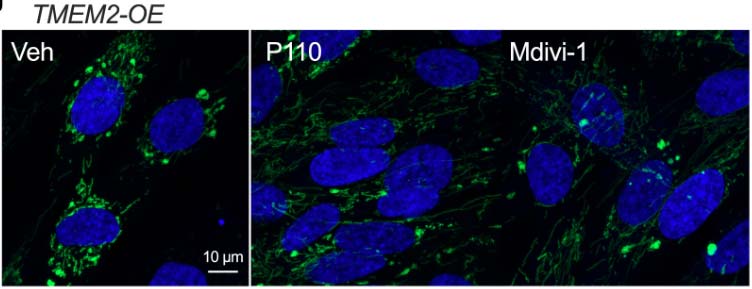
图10:抑制剂对线粒体碎片化的改善

TMEM2-OE通过TGF-β通路显著上调Ⅰ型干扰素等抗病毒免疫基因。TMEM2/TGF-β1诱导线粒体膜完整性破坏,导致mtDNA泄漏至胞质,后者可能通过cGAS-STING通路激活免疫反应。
在线虫模型中,hTMEM2-OE增强了对病原菌感染的抵抗力,且肠道特异性表达即有效。该保护作用依赖UPRMT(ATFS-1)和抗氧化反应(SKN-1)通路,而非干扰素通路。有趣的是,hTMEM2并非通过清除病原体,而是通过增强宿主对病理损害的耐受能力来提供保护。
研究还发现,hTMEM2对E. faecalis(革兰氏阳性)的保护效果强于S. marcescens(革兰氏阴性)。发现E. faecalis能强力诱导UPRMT并降解宿主ECM(软骨素减少)。说明这项发现提出了一个精妙的“预警-增强”模型:某些病原菌(如E. faecalis)会分泌酶来攻击宿主的ECM屏障以利于入侵。TMEM2的活性可能模拟了这种攻击,提前激活了线粒体应激免疫通路,使宿主在真正的感染到来时已准备就绪,从而实现了更强的耐受性。
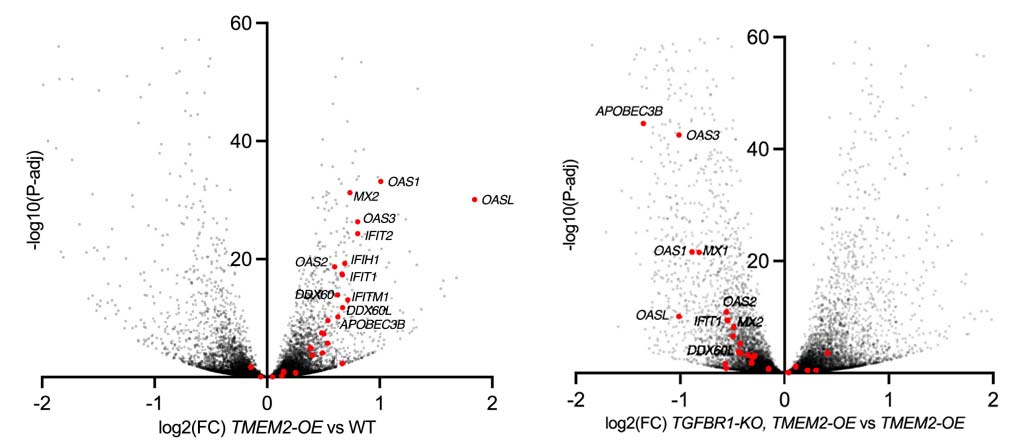
图11:对野生型(WT)、TMEM2过表达(TMEM2-OE)及TGFBR1敲除的TMEM2过表达成纤维细胞进行RNA测序分析,抗病毒反应基因被标红突出显示。

这项研究彻底改变了我们对ECM功能的认识,揭示了一条从ECM到线粒体的精确信号通路:TMEM2介导的HA降解通过激活TGF-β-SMAD通路,上调线粒体分裂基因表达,导致线粒体功能紊乱,同时增强了机体的免疫防御能力。这条"ECM-HA-TGF-β-线粒体"轴的发现,为理解细胞微环境与细胞器功能间的对话提供了全新范式,也为治疗线粒体功能障碍相关疾病和感染性疾病提供了新的潜在靶点。未来,通过调控这一通讯轴,或许能够实现精准改善线粒体健康和提高免疫能力的目标。
本文作者:张程。Bioπ中国美肤科学传播平台发布本文只是为了更多的信息参考,不代表任何有倾向性的投资意见或市场暗示。
THE END

京公网安备11010502058609号





















