科学公报
HA受体CD44信号通路在皮肤修复与再生的作用
2025年12月14日 16:37

透明质酸(HA)自1934年被首次提取以来,一直在医美领域中扮演着重要角色。
华熙生物自1990年创立以来,已成为全球知名的合成生物科技创新驱动的生物科技公司和生物材料全产业链平台公司。依托其强大的基础研究和应用基础研究为核心,创造新物质。同时拥有全球最大的中试转化基地,完成从细胞构建到商业应用的产品全生命周期。作为生物材料全产业链平台公司,主要聚焦于人类健康相关的功能糖、蛋白质、多肽、氨基酸、 核苷酸、天然活性化合物等生物活性物质,实现研发、生产及销售的一体化。秉承“让每个生命都是鲜活的”企业使命,为人类持续带来健康、美丽、快乐的生命体验——提高生命质量、延长生命长度。
华熙学苑文献解读将探索HA的独特之处,展示其在医美中的核心作用和巨大价值。


皮肤创伤后的愈合过程往往伴随瘢痕形成,尤其是增生性瘢痕(HTS)的防治仍是临床难题。现有疗法对瘢痕的改善效果有限,其核心原因在于对伤口愈合各阶段(止血、炎症、增殖、重塑)的调控机制尚未完全阐明。研究发现,组织损伤后,CD44受体及其特异性配体透明质酸(HA)的表达显著上调,提示二者构成的信号轴可能在伤口愈合中发挥关键作用。
然而,CD44与不同分子量HA的相互作用如何影响炎症平衡、细胞功能及瘢痕形成,以及如何通过调控该信号轴实现无瘢痕再生,尚未形成系统认知。为此,来自美国约翰・霍普金斯大学、迈阿密BioTissue公司等机构的研究团队在《Journal of Translational Medicine》发表综述,首次系统梳理了CD44信号在皮肤伤口愈合中的多重作用,重点解析了不同分子量HA对CD44功能的调控差异,并提出通过人羊膜来源的HC-HA/PTX3复合物激活CD44再生潜能的新范式,为瘢痕防治和再生医学提供了理论依据。
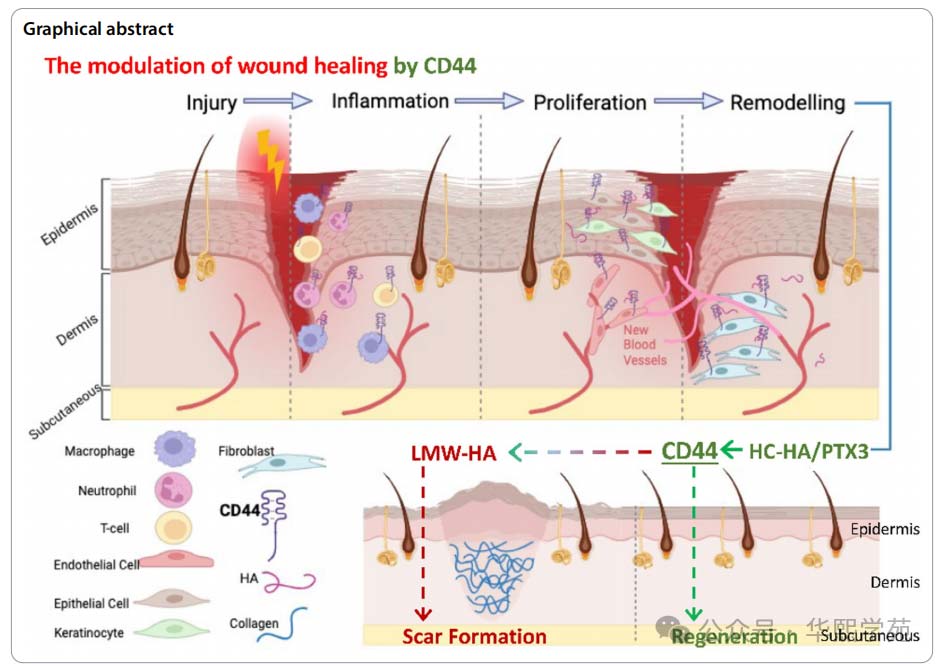


CD44是一种广泛表达于脊椎动物细胞表面的非激酶跨膜糖蛋白,其结构包括胞内域、跨膜域和胞外域(含N端配体结合位点),可通过胞内外域的相互作用介导细胞与外界环境的信号传递。
CD44存在两种主要异构体:
1. 标准型(CD44s):由恒定外显子编码,主要通过胞外域结合HA,调控细胞增殖、黏附和迁移等基础功能。
2. 变异型(CD44v):通过可变外显子(6-15号)剪接形成,除结合HA外,还可作为共受体与细胞因子(如HGF)、生长因子(如VEGF)结合,激活c-Met、VEGFR-2等受体酪氨酸激酶信号通路,参与复杂的组织重塑过程。
异构体的转换(如CD44v向CD44s转换)由异质核核糖核蛋白M(hnRNPM)介导,受上皮剪接调节蛋白1(ESRP1)负调控,这一过程与上皮-间质转化(EMT)密切相关,在伤口纤维化和瘢痕形成中起重要作用。

CD44与HA的结合存在三种亲和力状态:
1. 静息态:无法与HA结合;
2. 可诱导激活态:受细胞因子、生长因子等外界刺激后转为激活态;
3. 持续激活态:无需外界刺激即可高亲和力结合HA。
激活后,CD44通过以下机制调控细胞功能:
与HA结合后引发膜定位改变,激活PI3K/AKT、RhoGTPases等下游信号通路,影响细胞增殖与迁移;
与Ezrin-Radixin-Moesin(ERM)家族蛋白结合,介导细胞骨架重组,参与伤口收缩与血管生成。



CD44广泛表达于中性粒细胞、巨噬细胞、T细胞等免疫细胞表面,通过调节其功能影响炎症的启动与消退。
1. 中性粒细胞:CD44通过与HA、PSGL-1结合,介导中性粒细胞与血管内皮的黏附及向伤口迁移;激活后还可通过释放Galectin-9调节T细胞活性。LMW-HA可通过CD44放大中性粒细胞的炎症反应,而HC-HA/PTX3则促进活化中性粒细胞凋亡,避免炎症过度。
2. 巨噬细胞:CD44通过调节软骨素硫酸化修饰影响HA结合能力——M1型巨噬细胞(促炎)的CD44硫酸化水平低,与HA结合增强,释放促炎因子;M2型巨噬细胞(抗炎)则相反,通过IL-10等因子促进炎症消退。HMW-HA和HC-HA/PTX3可诱导巨噬细胞向M2型极化,而LMW-HA则维持M1型表型。
3. T细胞:CD44是记忆T细胞的标志,通过与Lck激酶结合增强T细胞受体信号,促进其活化与增殖。HC-HA/PTX3可通过CD44抑制CD4+T细胞活化,同时促进调节性T细胞(Tregs)扩增,减轻适应性免疫反应引发的组织损伤。

1. 角质形成细胞与上皮再生:CD44(尤其是CD44v3-v10)通过与层粘连蛋白332、syndecan-1相互作用,调控角质形成细胞的迁移、增殖及表皮屏障修复。HA激活的CD44可通过RhoGTPases信号促进细胞骨架重组,加速伤口再上皮化。
2. 血管内皮细胞与血管新生:CD44通过与寡聚HA(O-HA)、ERM蛋白结合,促进血管内皮细胞的管腔形成和F-肌动蛋白分支,是伤口血管生成的关键调控因子。CD44缺失会导致血管内皮细胞排列紊乱,影响新生血管完整性。
3. 成纤维细胞与纤维化:CD44s(鼠源)和CD44v(人源)通过结合纤连蛋白、乳酸等分子,调控成纤维细胞向伤口迁移;其与TGF-β1的正反馈环路可促进成纤维细胞向肌成纤维细胞分化(α-SMA表达上调),参与胶原沉积。HC-HA/PTX3可通过抑制该环路减少纤维化,甚至使肌成纤维细胞逆转为正常成纤维细胞。


HA的分子量是决定CD44功能的关键因素,不同分子量HA通过CD44介导的生物学效应截然不同:
1. 高分子量HA(HMW-HA,>1000kDa):通过交联CD44形成簇状结构,激活抗炎、抗纤维化信号,促进M2型巨噬细胞极化和正常组织结构恢复,与胎儿无瘢痕愈合密切相关。
2. 低分子量HA(LMW-HA,<500kDa):通过单体CD44激活TLR4/NF-κB通路,诱导促炎因子释放(如IL-1β、TNF-α),促进中性粒细胞浸润和肌成纤维细胞分化,加剧瘢痕形成。
3. 寡聚HA(O-HA,6-22mer):作用具有双重性,6-8merO-HA可通过CD44促进伤口闭合,但高浓度时可能激活炎症反应,其机制仍需进一步明确。
4. HC-HA/PTX3复合物:由人羊膜来源的HMW-HA与重链1(HC1)、五聚蛋白3(PTX3)组成,是激活CD44再生功能的新范式。其通过CD44抑制炎症、减少纤维化,并促进干细胞静息与自我更新,在角膜修复、疼痛缓解等方面已显示出优异效果。
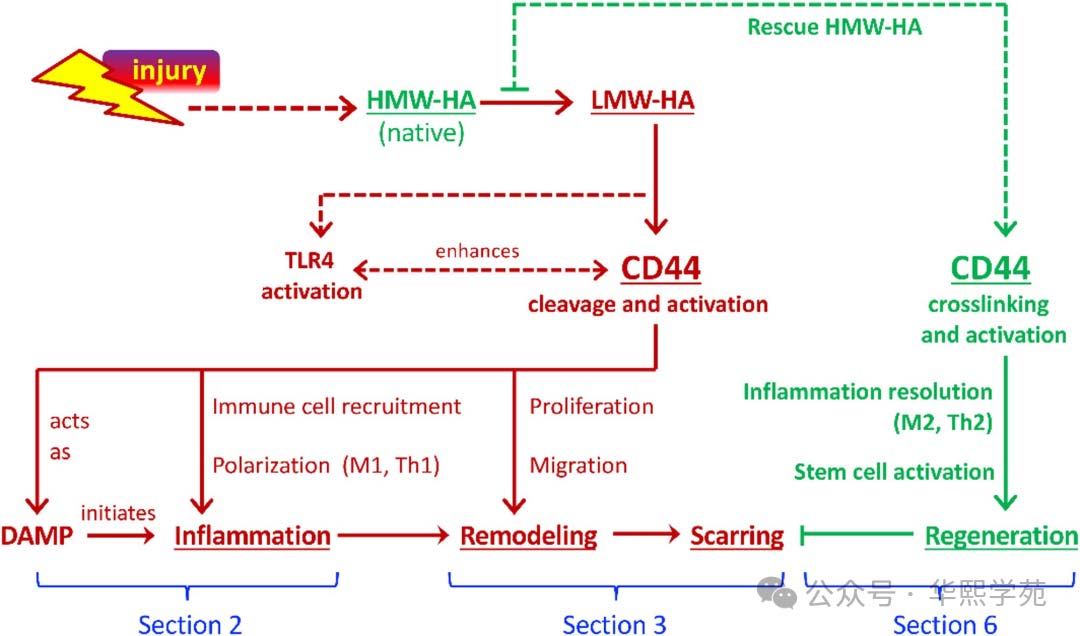
图1:不同分子量透明质酸(HA)激活的CD44信号在伤口愈合中作用的示意图。
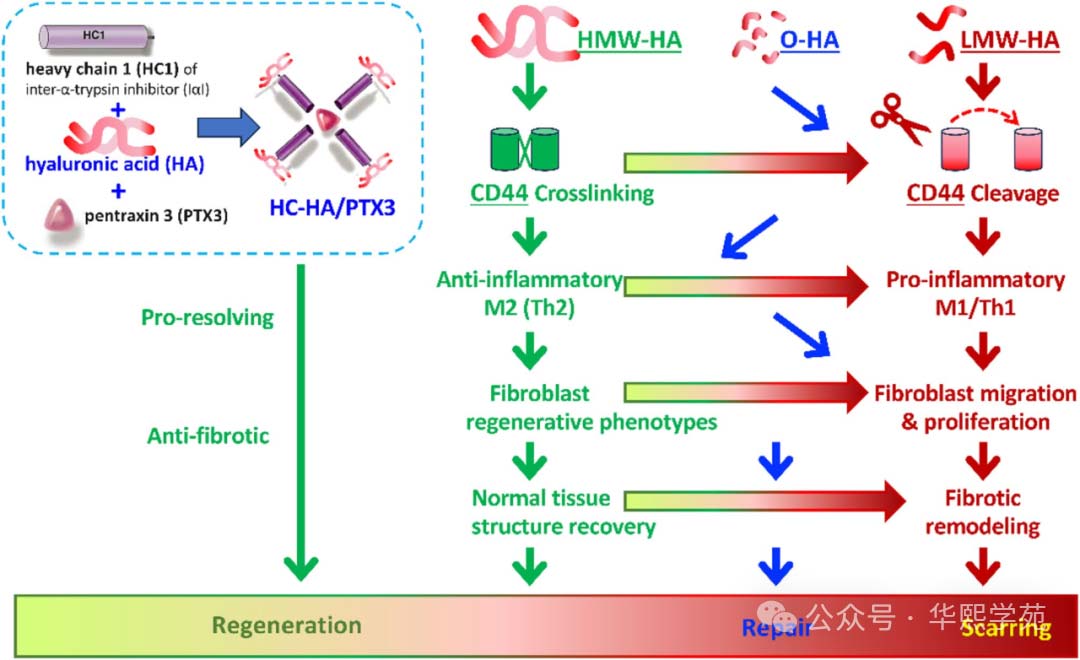
图2:在各种分子量的透明质酸及含透明质酸的复合物调控下,CD44在伤口愈合中发挥多种功能。


高血糖通过透明质酸酶降解HA,减少CD44配体,导致血管内皮细胞NO生成减少、细胞骨架紊乱,延缓愈合。激活CD44信号(如补充HA)可改善血管功能,促进糖尿病伤口修复。

老年皮肤HA含量降低,尤其是<300kDa的HA缺失。250kDaLMW-HA可通过CD44促进胶原I/III表达,加速老化伤口愈合;而HMW-HA则通过CD44延缓皮肤衰老,维持组织弹性。

银屑病皮损中CD44表达下调,LMW-HA通过CD44加剧表皮炎症;烧伤伤口中CD44与MMP-9高表达相关,可能延缓愈合,提示调控CD44信号可改善此类慢性伤口预后。
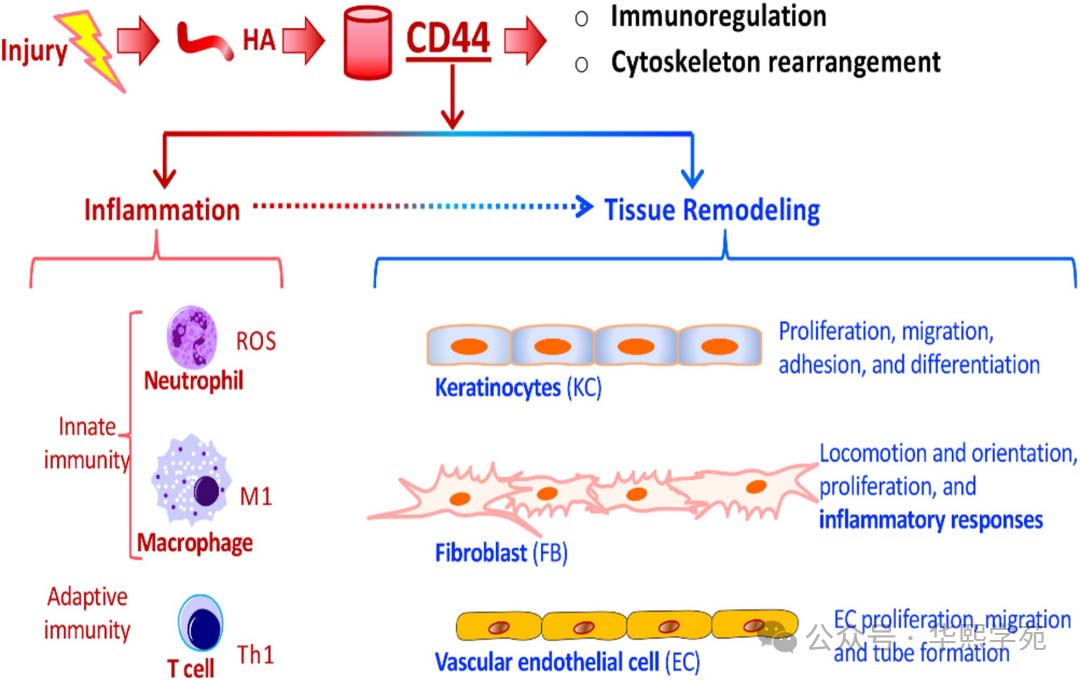
图3:CD44在皮肤伤口愈合中调节炎症和组织重塑的细胞机制。
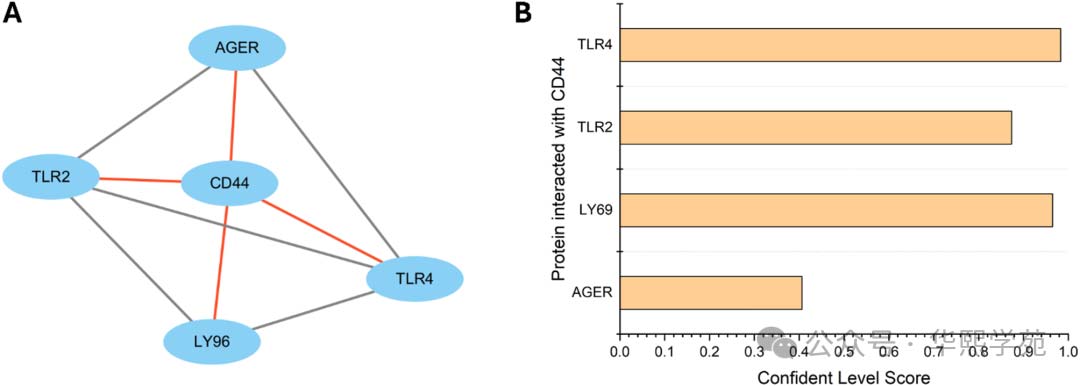
图4:CD44与DAMP相关蛋白的相互作用。

CD44是干细胞(如间充质干细胞、表皮干细胞)的标志物,通过以下机制促进皮肤再生:
介导干细胞向伤口迁移、定植,增强其增殖与分化能力;
与骨桥蛋白结合激活HIF1A/CREBBP通路,促进毛囊再生;
HC-HA/PTX3通过CD44维持干细胞多能性,为再生提供细胞来源。
动物实验证实,CD44+干细胞移植可加速全层皮肤缺损的愈合,减少瘢痕并促进毛发再生,为临床再生疗法提供了实验依据。
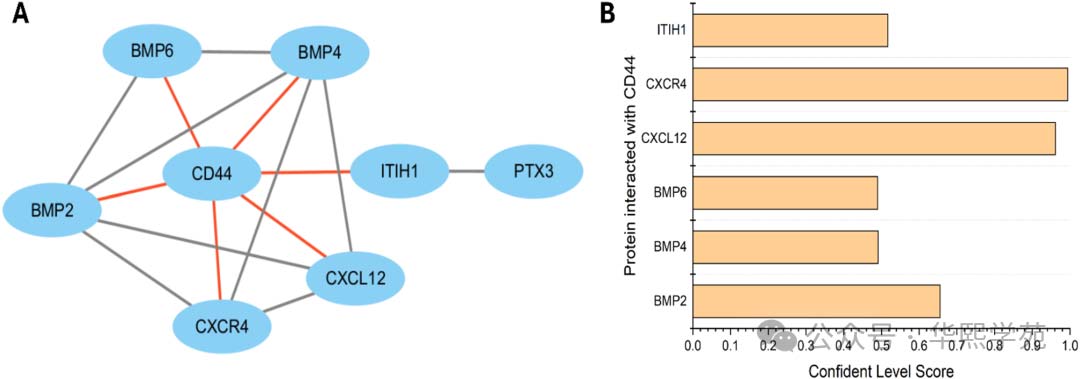
图5:CD44与HC-HA/PTX3相关蛋白的相互作用。
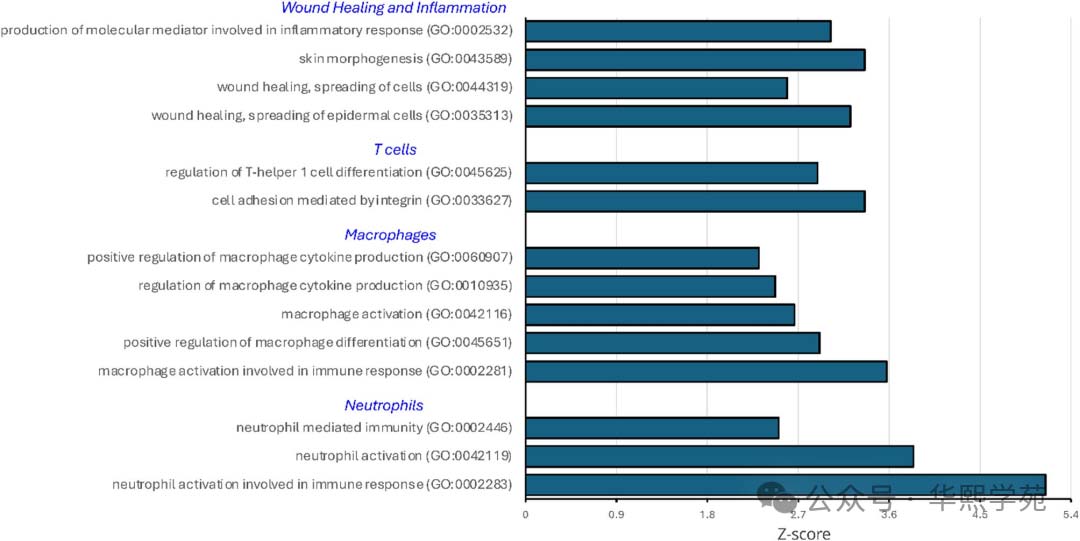
图6:与伤口愈合相关的CD44介导的生物学过程分析。

该综述系统阐明了CD44信号在皮肤伤口愈合中的核心作用:作为HA的主要受体,CD44通过调控免疫细胞功能、细胞增殖与迁移、纤维化等过程,贯穿伤口愈合的全阶段;其功能受HA分子量严格调控——HMW-HA和HC-HA/PTX3通过CD44促进抗炎与再生,LMW-HA则倾向于引发炎症与瘢痕。研究的核心价值在于:揭示了CD44异构体转换、HA分子量差异对愈合结局的影响,为靶向干预提供了分子靶点;提出HC-HA/PTX3激活CD44再生功能的新策略,为无瘢痕愈合开辟了新路径;明确了CD44在糖尿病、老化等特殊伤口中的作用,为个性化治疗提供了依据。
未来研究需进一步探索CD44下游特异性效应分子,优化HA/HC-HA/PTX3的递送方式,推动其从基础研究向临床转化,最终实现皮肤伤口的再生性修复。
参考文献:
[1] Guan, A. Y., Chen, Y., Tseng, S. C., & Lin, Q. CD44 signaling in skin wound healing and regeneration. Journal of Translational Medicine, 2025, 23:880. https://doi.org/10.1186/s12967-025-06913-5.
来源:华熙学苑。Bioπ中国美肤科学传播平台发布本文只是为了更多的信息参考,不代表任何有倾向性的投资意见或市场暗示。
THE END

京公网安备11010502058609号





















