探讨与争鸣
青春逆转密码
ECM抗衰全景图
2025年08月07日 12:39

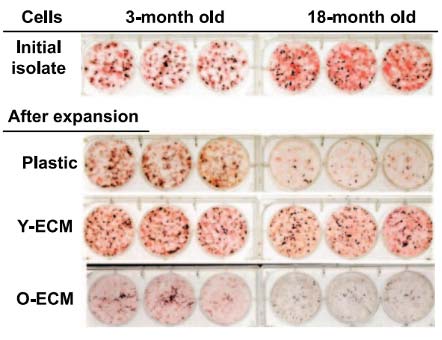
2011年,中美科研团队联合研究发现,老化的间充质干细胞(MSC,Mesenchymal stem cell)在年轻小鼠骨髓细胞外基质(ECM,Extracellular maxtrix)中培养后,在增殖能力和抗氧化水平等多个尺度上恢复“年轻化”(图1)1。ECM“逆天改命”的抗衰能力早有端倪,随着生命科学技术的迅速迭代,海量的前沿研究也佐证了ECM对维持细胞稳态和促进机体健康的强大能力。2025年4月,法国索邦大学衰老领域研究专家在国际顶尖学术期刊Cell上正式提出,细胞外基质变化是衰老的第十三大标志2。ECM成分和结构的改变,能够通过粘弹性变化、线粒体稳态、细胞衰老及干细胞活性等多种机制,深刻影响机体衰老过程。这些发现为我们提供了新的思路:如何深入挖掘ECM相关的皮肤抗衰靶点,从而探索并建立全新的抗衰策略?

了解ECM的组成和结构是破译ECM抗衰密码的第一步。ECM主要由胶原蛋白、蛋白聚糖、弹性蛋白和细胞黏附性糖蛋白等大分子组成。其中,胶原蛋白是最丰富的结构蛋白,它以三螺旋形态形成纤维,为组织提供拉伸强度;弹性蛋白则赋予组织弹性。蛋白聚糖中最具代表性的是透明质酸(HA,Hyaluronic acid),它能大量吸水,保持细胞外空间的润滑和弹性。可以说,胶原蛋白与透明质酸是ECM抗衰老的重要“双子星”:胶原为组织搭建骨架,HA则保持环境湿润饱满。
在皮肤组织中,ECM占据了极高比例,真皮层中ECM体积占比80%以上。胶原蛋白是皮肤ECM的主要成分,约占ECM蛋白质总量的70%。斯坦福大学的研究团队对18-95岁的4263名受试者的血浆蛋白组进行分析,发现在大约34岁这个阶段,以胶原蛋白为主的ECM蛋白组分大幅下降,提示ECM成分减退是衰老的重要标志之一3。事实上人们对于补充胶原蛋白来抵御衰老的追求一直从未停歇,然而单一的胶原蛋白补充策略治标不治本,衰老或者功能异常的成纤维细胞会持续分泌基质金属蛋白酶(MMPs,Matrix metalloproteinases)降解胶原蛋白和弹性蛋白4。这也提示改善细胞自身功能或代谢状态或者长效抗衰的更优解。
透明质酸(HA)是一种高度亲水的糖胺聚糖,能够结合并保持大量水分。在皮肤ECM中,透明质酸负责维持基质水润度和黏弹性,使皮肤饱满有弹性。随着年龄增长,皮肤HA含量下降,皮肤失水瘙饿而出现皱纹。HA已被证明可通过涂抹和皮肤填充注射的方式吸引水分增加皮肤体积,从而填平皱纹、改善面部轮廓。
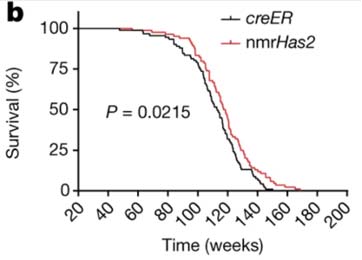
HA不仅帮助对抗肌肤衰老,还被证明促进哺乳动物的寿命延长。一项来自国际顶级期刊Nature的研究中,科学家将裸鼹鼠中的透明质酸合成酶2基因(Has2)导入普通小鼠,产生了高分子量HA的小鼠模型(nmrHAS2小鼠)。这些转基因小鼠体内多组织HA含量显著增加,相比对照组自发性肿瘤发生率大幅降低,寿命延长且健康寿命改善5(图2)。具体表现为年老小鼠出现炎症反应减弱(多组织慢性炎症明显减少)、肠道屏障功能增强。此外,这些小鼠在肌肉和骨骼方面也显示出更好的功能,如老年小鼠骨连接密度更高,衰老相关的组织退化减缓。
总之,胶原蛋白和透明质酸在物理支撑层面协同维护组织结构:胶原纤维构成主要的力学骨架,提供强度与支持;透明质酸则通过强大的保水能力保持基质水润和黏弹性,协助吸震缓冲,同时缓解多组织的慢性炎症。自然衰老过程中,胶原和HA双双下降导致ECM支撑力减弱和组织萎缩。因而,保持胶原蛋白结构和补充HA有助于延缓皮肤和组织衰老,这一“支撑-保湿”协同机制对于抗衰老具有重要意义。


除了物理层面的支撑和水分保持,ECM还通过一系列信号通路影响细胞的命运,包括改变机械力和线粒体稳态。随着年龄增长,组织中的ECM发生显著变化:胶原纤维的交联增强、弹性蛋白断裂降解、糖基化产物沉积增多,导致基质总体僵硬度提高,粘弹性下降。这种老化的ECM环境往往驱动细胞进入衰老状态,例如促进间质细胞的生长停滞和对正常凋亡程序的耐受,表明ECM结构的改变可能是细胞衰老和组织功能退化的重要诱因。
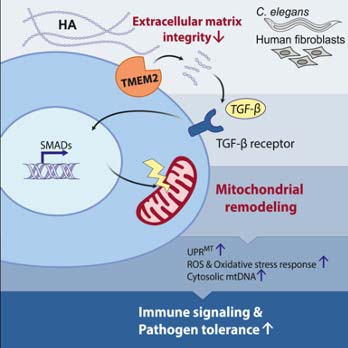
近期发表于Cell的研究进一步揭示,ECM的力学重塑会通过TGF-β信号通路影响线粒体稳态。由于环境或者遗传因素导致高分子量HA降解,ECM 重塑后释放的信号可激活TGF-β通路,诱导线粒体裂变和线粒体蛋白折叠应答(UPR^MT),增强线粒体应激反应(图3)6。换言之,基质力学信号可以传递到线粒体层面,协调细胞的代谢和免疫防御。另一方面,当ECM过于僵硬或受损时(如紫外线损伤导致的基质变化),成纤维细胞的线粒体功能受到抑制,ATP合成下降,其分泌的胶原蛋白和弹性蛋也明显减少。细胞外基质的崩解进一步恶化了细胞生存环境,皮肤陷入ECM破坏-细胞衰老或损伤的恶性循环。

鉴于ECM在介导皮肤衰老的“枢纽”作用,在传统的ECM补充方法之外,通过直接恢复细胞自身功能来延缓组织衰老,是打破ECM耗竭和细胞之间恶性循环的有效策略,这也与近年来火热的“细胞级抗衰”概念遥相呼应。这种策略强调通过激活细胞内能量代谢和线粒体功能,重建衰老细胞的年轻状态,从而驱动ECM成分的再生达到细胞层级抗衰或者终止恶性循环。例如,线粒体功能受损(如ATP供给不足)会直接导致成纤维细胞分泌的胶原和弹性蛋白减少;相反,提升线粒体活性(如增加NAD+供应、激活自噬清除受损线粒体等)则有望恢复细胞的胶原合成能力。通过这种方式,细胞“重获活力”不仅可促进自身线粒体和代谢功能的改善,也能增强胶原纤维与弹性纤维的生成,实现更深层次、系统性的抗衰效果。换言之,“细胞级抗衰”强调从细胞代谢的源头出发,全面激发细胞活性,以细胞功能的提升带动基质更新。
综上所述,除了传统的外源补充ECM(如填充剂、保健品)之外,细胞级抗衰策略通过激发细胞自身的活力来促进ECM的内源合成,从而形成有益的正反馈循环:活跃的成纤维细胞产生更多的胶原和弹性蛋白,良好的ECM环境反过来又支持细胞增殖和修复能力。这种细胞–基质互作的良性循环有望从根本上重塑老化组织的功能态,驱动组织向年轻化方向转变。未来抗衰老研究应进一步探索这一网络中的关键靶点,通过综合干预细胞能量代谢和基质修复,为延缓衰老和组织再生提供新思路和策略。
参考文献
1. Sun, Y., Li, W., Lu, Z., Chen, R., Ling, J., Ran, Q., Jilka, R.L., and Chen, X.D. (2011). Rescuing replication and osteogenesis of aged mesenchymal stem cells by exposure to a young extracellular matrix. FASEB J 25, 1474-1485.
2. Kroemer, G., Maier, A.B., Cuervo, A.M., Gladyshev, V.N., Ferrucci, L., Gorbunova, V., Kennedy, B.K., Rando, T.A., Seluanov, A., Sierra, F., et al. (2025). From geroscience to precision geromedicine: Understanding and managing aging. Cell 188, 2043-2062.
3. Lehallier, B., Gate, D., Schaum, N., Nanasi, T., Lee, S.E., Yousef, H., Moran Losada, P., Berdnik, D., Keller, A., Verghese, J., et al. (2019). Undulating changes in human plasma proteome profiles across the lifespan. Nat Med 25, 1843-1850.
4. Butler, G.S., and Overall, C.M. (2009). Updated biological roles for matrix metalloproteinases and new "intracellular" substrates revealed by degradomics. Biochemistry 48, 10830-10845.
5. Zhang, Z., Tian, X., Lu, J.Y., Boit, K., Ablaeva, J., Zakusilo, F.T., Emmrich, S., Firsanov, D., Rydkina, E., Biashad, S.A., et al. (2023). Increased hyaluronan by naked mole-rat Has2 improves healthspan in mice. Nature 621, 196-205.
6. Zhang, H., Tsui, C.K., Garcia, G., Joe, L.K., Wu, H., Maruichi, A., Fan, W., Pandovski, S., Yoon, P.H., Webster, B.M., et al. (2024). The extracellular matrix integrates mitochondrial homeostasis. Cell 187, 4289-4304 e4226.
本文作者:费照亮、朱军进,编辑发布时有略微删减。Bioπ中国美肤科学传播平台发布本文只是为了传递更多的信息,不代表有任何倾向性的暗示或意见,仅供读者参考。
THE END

京公网安备11010502058609号





















