皮肤科普
外泌体 miR-302b:
让衰老 “逆龄”的秘密
2025年09月25日 06:51

衰老是生命进程中不可避免的生理现象。随着年龄增长,细胞逐渐丧失增殖潜能并累积功能缺陷,进而引发多种衰老相关疾病。科学界持续探索延缓衰老的策略,包括热量限制、衰老细胞清除及基因治疗等。然而,如何在安全、可控的前提下有效逆转衰老状态,仍是当前领域面临的重大挑战。
2025 年,Cell Metabolism 发表了一项突破性研究,题为《Exosomal miR-302b rejuvenates aging mice by reversing the proliferative arrest of senescent cells》。研究发现,一种来源于人胚胎干细胞外泌体的 microRNA——miR-302b,能够恢复衰老细胞的增殖能力,从而显著延缓小鼠的衰老进程。这为未来皮肤抗衰老干预提供了新的思路。

科学家们在一项令人兴奋的研究中发现,人类胚胎干细胞来源的外泌体(hESC-Exos)拥有让衰老细胞“重返青春”的强大能力。研究人员选取了人类成纤维细胞IMR-90作为研究对象。这种细胞在分裂大约50代后会进入不可逆的衰老状态,停止增殖。实验将这种衰老细胞分为两组,一组用hESC-Exos进行处理,另一组作为对照。72小时后,观察到经hESC-Exos处理后的衰老IMR-90细胞表现出多方面的“年轻化”逆转特征:衰老相关β-半乳糖苷酶(SA-β-gal)活性降低(图1a),衰老及相关分泌表型(SASP)基因(如CDKN2A、CDKN1A、IL-1a、IL-11和CCL20)的表达下调。在群体倍增实验中,细胞增殖能力明显增强,增殖标志物Ki67的表达量上升(图1b),处于S期的细胞比例也显著提高(图1c)。进一步的RNA测序(RNA-seq)分析显示,hESC-Exos显著抑制了衰老相关基因(如TP53、IL-6、CDKN1A和CDKN2A)的表达,同时促进了增殖相关基因(包括MKI67、PCNA、TOP2A和CDK1)的表达(图1d)。差异表达基因(DEG)功能注释表明,上调基因多与有丝分裂细胞周期和细胞周期进程相关,而下调基因则富集于细胞衰老和炎症反应通路。基因集富集分析(GSEA)进一步证实,hESC-Exos处理增强了细胞周期相关通路的富集程度。这些结果一致表明,hESC-Exos能够使衰老的IMR-90细胞恢复年轻状态,并重新获得增殖潜力。
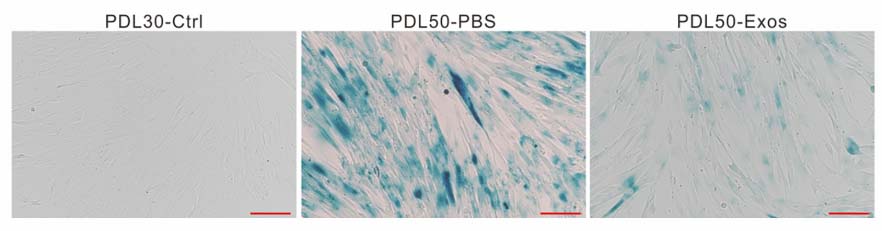
图1a:hESC-Exos处理后的衰老IMR-90细胞表现SA-β-gal活性降低
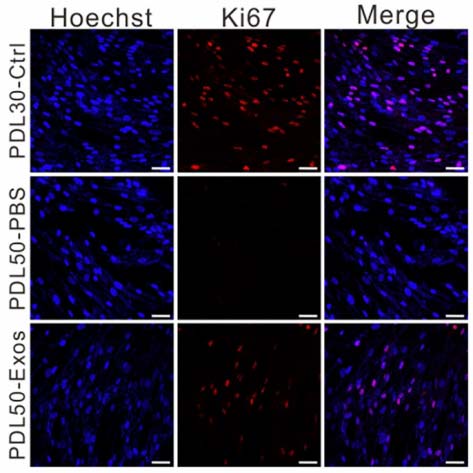
图1b:hESC-Exos处理后的衰老IMR-90细胞增殖标志物Ki67的表达量上升
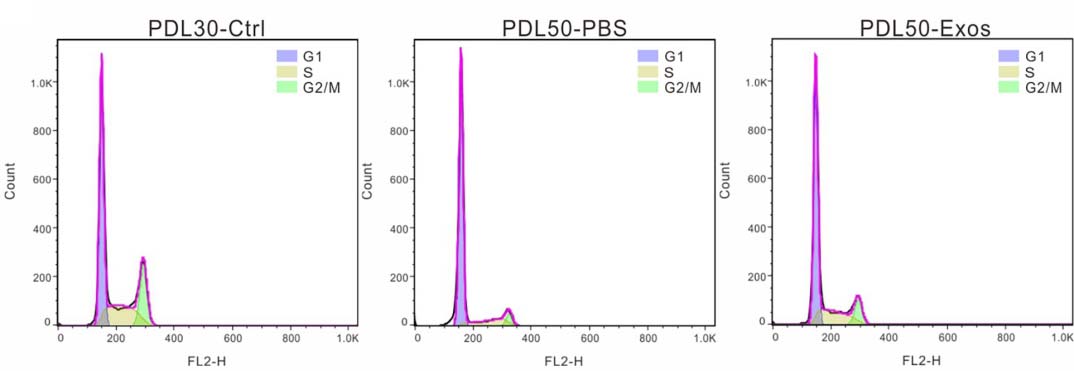
图1c:hESC-Exos处理后的衰老IMR-90细胞处于S期的细胞比例显著提高
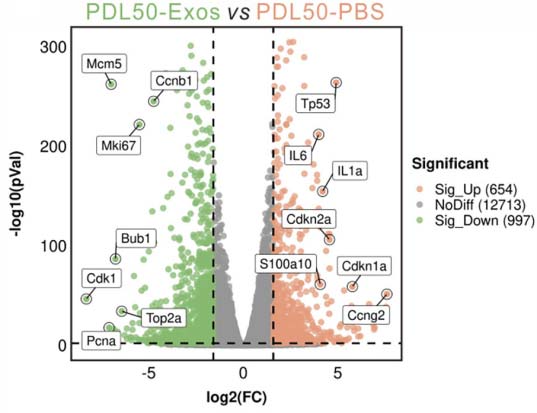
图1d:hESC-Exos处理后的衰老IMR-90细胞RNA测序(RNA-seq)分析

为了在单细胞层面上看清hESC-Exos究竟如何让衰老细胞“重获新生”,研究人员通过将黄色荧光蛋白(YFP)基因插入 CDKN1A(编码 p21)终止密码子下游构建了一个“衰老报告系统”:当细胞衰老时发出荧光,这样就可以轻松地找到并分离出这些衰老细胞。当用hESC-Exos处理这些衰老细胞后, YFP 信号和 SA-β-gal 活性被抑制,同时,代表增殖能力的Ki67蛋白信号增强。更直观的是,活细胞成像直接捕捉到,部分原本“躺平”不分裂的衰老细胞,在治疗后重新开始了增殖分裂,说明hESC-Exos使部分衰老细胞重新进入增殖过程。单细胞 RNA 测序分析显示,hESC-Exos处理组中处于DNA合成期(S期)的细胞比例增加了17%(图2a)。
根据已报道的增殖和衰老标志物对细胞簇进行注释,将MKI67和PCNA高表达的细胞定义为 rejuvenated 细胞(Rej),CDNK1A和TP53高表达的细胞为衰老细胞(Sen),其余为中间状态细胞(Int)。结果显示,与Dox-PBS相比,Dox-Exos组Rej细胞比例增加,同时Sen细胞比例减少。通过鉴定沿伪时序轨迹从Int向Sen以及Int向Rej转变过程中的差异表达基因(DEGs),Int向Rej分化过程中上调的基因包括CENPF、SERBP1和TOP2A,这些基因在有丝分裂过程中富集。Int向Sen分化过程中上调的基因,如CCNG2、CDKN1C和CDKN2A,这些基因参与细胞衰老和SASP的调控(图2b)。综上所述,hESC-Exos处理逆转了单个衰老细胞的增殖停滞,使其重新获得增殖能力。
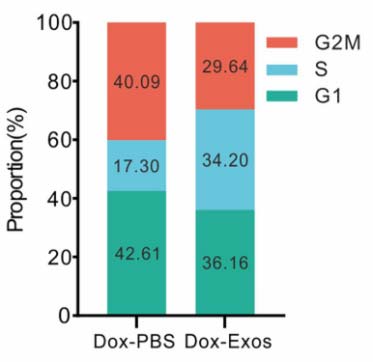
图2a:统计S期细胞的比例
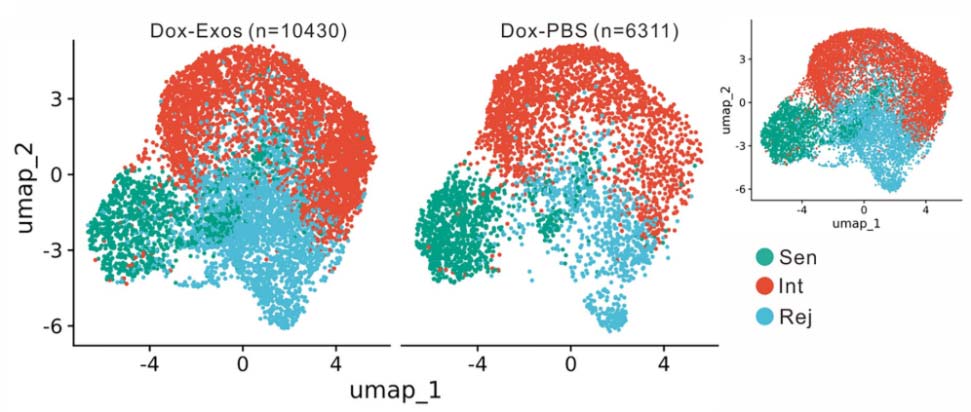
图2b:统计Rej,Sen,Int细胞的比例

hESC-Exos 治疗可逆转老年小鼠的衰老表型并部分恢复其增殖能力。在老年小鼠中,hESC-Exos 处理显著延长了中位和最大寿命,改善了毛发稀疏、运动能力下降、认知功能障碍等衰老相关表型,并降低了血清中促炎细胞因子(如 IL-1β、IFN-γ、IL-6 和 TNF-α)的水平。组织学分析显示,hESC-Exos 减少了衰老相关β-半乳糖苷酶(SA-β-gal)阳性细胞及DNA损伤标志物γ-H2AX的表达,同时提高了基因组稳定性标志物H3K9me3的水平。
从机制上讲,通过肝脏和皮肤组织的单细胞转录组分析发现,hESC-Exos 处理恢复了衰老组织中S期细胞比例,并鉴定出一组被称为“救援细胞周期相关基因(rescue CCGs)”的关键基因。其中,Cdkn2a、Cdkn1a、Cdkn1b 和 Ccng2 表达下调,而 E2f1、Mki67、Top2a、Cdk1、Ccnb1 和 Pcna 表达上调。伪时序轨迹分析进一步表明,hESC-Exos 推动了细胞从衰老状态(Sen)向再生状态(Rej)转变,其中肝脏组织中 Selenop、Pcna、Mki67 和 Top2a 等基因上调,而皮肤组织中 Krt15、Mki67 等基因上调,同时 Cdkn1a 和 Ccng2 在两个组织中均被抑制(图3)。这些结果说明,hESC-Exos 处理逆转了 SnC 的细胞周期停滞,从而通过抑制 Cdkn1a 和 Ccng2 的表达来促进年轻化。
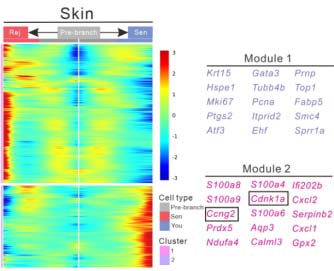
图3:基因共表达模块及各模块的示例基因

hESC-Exos 封装了参与衰老过程的多种生物活性物质,那么具体那个核心物质起到作用呢?作者通过高通量测序发现miR-302b-3p在hESC-Exos中显著富集。通过绝对定量PCR测定,其浓度被精准定标为每1000个hESC-Exos颗粒中含(306 ± 50.6)pmol。
为进一步解析其功能机制,我们通过Ago2 Clip-seq分析鉴定出miR-302b的靶基因,并发现其结合位点与miRanda和TargetScan预测结果高度重叠。基因本体(GO)分析显示,这些靶基因主要富集于有丝分裂细胞周期、细胞分裂和DNA损伤应答等过程。值得注意的是,miR-302b与Cdkn1a和Ccng2的3′ UTR具有较低的最小自由能(MFE),分别为-12.84和-16.15 kcal/mol,表明结合是特异且高效的。双荧光素酶报告实验证实,miR-302b可特异性靶向Cdkn1a和Ccng2的3′ UTR并显著抑制其荧光活性。在小鼠实验中,与衰老PBS组相比,hESC-Exos处理的老年小鼠肝和皮肤组织中miR-302b水平显著上升,同时伴随Cdkn1a和Ccng2表达的下降。
为验证miR-302b单独是否足以逆转衰老,作者在PDL50 IMR-90衰老细胞中转染miR-302b模拟物。结果显示,过表达miR-302b可显著降低SA-β-gal活性,提高S期细胞比例,并下调p21和Ccng2的蛋白水平。综上所述,作者推断miR-302b通过在体外抑制Cdkn1a和Ccng2的表达来促进年轻化。

为探究miR-302b的体内 rejuvenation 效应,研究通过电转将miR-302b模拟物装载至293F细胞来源的外泌体中,构建Exos-302b递送系统。25月龄老年小鼠经Exos-302b连续干预5个月后,多项衰老表型得到显著改善:背部毛发再生增强、体重增加、运动协调能力(转棒实验)和抓力明显提升,空间学习与记忆能力(水迷宫实验)也显著优于对照组。
在分子层面,miR-302b干预有效缓解了老年小鼠的全身慢性炎症状态,并减少多个组织(肾、肝、肺、脾、皮肤)中衰老相关β-半乳糖苷酶阳性细胞的积累。此外,组织DNA损伤标志物γ-H2AX表达下降,而基因组稳定性标志物H3K9me3表达上升。绝对定量PCR显示,miR-302b在肝、皮肤及脑组织中大量富集,免疫荧光染色进一步证实其有效抑制了关键细胞周期检查点Cdkn1a和Ccng2的表达。
长期安全性评估表明,miR-302b干预显著延长老年小鼠中位寿命达137天(增加约15.4%),死亡风险比(HR)降至38%,最大寿命也显著延长。尽管寿命显著延长,两组小鼠在肿瘤发生率、疾病负担和死亡原因方面均无显著差异。病理学分析显示,miR-302b减轻了多器官的年龄相关性组织病变,包括皮肤角质化减少、脾脏白髓萎缩缓解等,并使增殖标志物Ki67的表达恢复至接近年轻小鼠水平。多组织转录组分析进一步表明,miR-302b能广泛恢复增殖相关信号并抑制炎症反应通路。因此,长期递送miR-302b可安全有效地延缓机体衰老,改善生理功能和组织稳态,延长健康寿命,且未增加肿瘤发生风险。
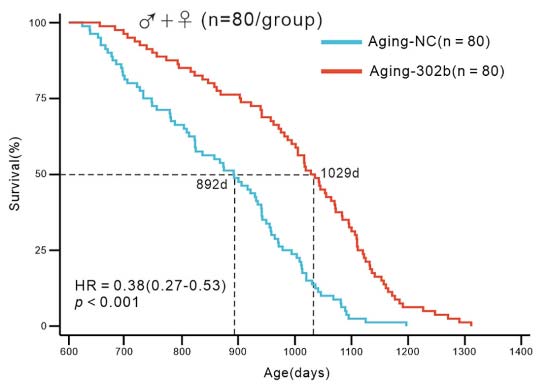
图4:生存曲线

这项研究揭示了外泌体封装的 miR-302b 能够通过靶向抑制细胞周期检查点基因 Cdkn1a 和 Ccng2,解除衰老细胞的增殖停滞,使其重新进入细胞周期,从而逆转了衰老相关表型并延长小鼠寿命。在实验中,miR-302b 不仅改善了小鼠的运动、认知等整体功能,还在皮肤组织层面显著降低了SA-β-gal和 DNA 损伤标志物 γ-H2AX 的积累,提升了 Ki67 等增殖因子的表达,恢复了组织结构的年轻化特征。这表明 miR-302b 不只是延缓表面老化,而是通过深层分子机制重建了皮肤的细胞稳态,为未来开发基于 miRNA 的皮肤抗衰干预策略提供了全新的科学依据。
本文作者:张程。Bioπ中国美肤科学传播平台发布本文只是为了更多的信息参考,不代表任何有倾向性的投资意见或市场暗示。
THE END

京公网安备11010502058609号





















